某10% NaOH溶液,加热蒸发掉100 g水后得到80 mL 20%的溶液,则该20% NaOH溶液的物质的量浓度为( )
| A.6.25 mol /L | B.12.5 mol /L | C.7 mol /L | D.7.5 mol /L |
下列说法中正确的是
| A.胶体区别于其他分散系的本质特征是丁达尔现象 |
| B.将小烧杯中25mL蒸馏水加至沸腾,向沸水中逐滴加入5~6滴氯化铁饱和溶液,继续煮沸至溶液呈红褐色沉淀,停止加热,以制取Fe(OH)3胶体 |
| C.Fe(OH)3胶体粒子在电场影响下将向阴极运动,说明Fe(OH)3胶体带正电 |
| D.往Fe(OH)3胶体中逐滴加入稀H2SO4溶液时,开始时会出现凝聚,再继续逐滴加时,沉淀又会消失 |
所谓合金,就是不同种金属(也包括一些非金属)在熔化状态下形成的一种熔合物,根据下列四种金属的熔沸点:根据表中数据判断,其中不能形成合金的是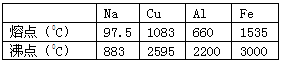
| A.Cu和Al | B.Fe和Cu | C.Fe和Na | D.Al和Na |
在无色透明溶液中可以大量共存的离子组是
| A.H+ Na+ S2- CO32- | B.H+ Ca2+ MnO4 NO3 NO3 |
C.K+Ca2+ Cl HCO3 HCO3 |
D.Cl Mg2+ Al3+ OH- Mg2+ Al3+ OH- |
下列离子方程式中正确的是
| A.H2SO4与Ba(OH)2溶液反应:Ba2++ OH-+ H++SO42-= BaSO4↓+ H2O |
| B.将稀硝酸滴加到氯化银固体上:AgCl + H+ = Ag+ + HCl |
| C.澄清的石灰水与稀盐酸反应:H++ OH- = H2O |
| D.大理石溶于醋酸的反应:CaCO3+ 2H+ = Ca2+ + CO2↑+ H2O |
只要用一种试剂,可区别NaCl、MgSO4、FeCl2、FeCl3四种溶液,这种试剂是
| A.HCl | B.NaOH | C.AgNO3 | D.BaCl2 |