某新型无机非金属材料A,由两种非金属元素组成,其中所含元素的化合价为其最高正价或最低负价,它是一种超硬物质,具有耐磨、耐腐蚀、抗冷热冲击、抗氧化的特征。A可由化合物B经下列反应制得:①B+NH3―→C[C的化学式为Si(NH2)4];②C经隔绝空气高温分解得到A。为探究B的组成,进行了下图所示的转化实验,图中G、F、H均为难溶于水的物质,且为白色粉末,图中字母代表的均为中学化学常见的物质。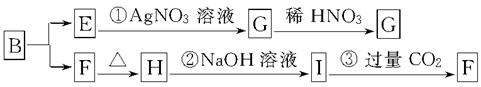
请回答下列问题:
(1)写出化合物B和化合物G的化学式______________、______________。
(2)A可能所属的晶体类型是________,在A晶体中,每个显正价原子周围结合的另一种原子的个数是________。
(3)写出反应②的离子方程式:____________________。
(4)写出C经隔绝空气高温分解得到A的化学方程式:________________。
(5)分析反应③,你能得出的结论是__________________________________________(合理即可)。
下表是元素周期表的一部分,回答下列有关问题(用化学符号回答):
| 族 周期 |
ⅠA |
ⅡA |
ⅢA |
ⅣA |
ⅤA |
ⅥA |
ⅦA |
0 |
| 2 |
① |
② |
③ |
|||||
| 3 |
④ |
⑤ |
⑥ |
⑦ |
⑧ |
⑨ |
||
| 4 |
⑩ |
(1)在①~⑩元素中,最活泼的金属元素是,最活泼的非金属元素是,最不活泼的元素是。
(2)在①~⑩元素的最高价氧化物对应的水化物中,酸性最强的是,碱性最强的是,呈两性的是。写出在水溶液中三者之间相互反应的离子方程式:,
,
。
用铜、银与硝酸银设计一个原电池,此电池的负极是:,
负极的电极反应式是:,
总反应方程式为。
在水溶液中,YO3-与S2-发生反应的离子方程式:YO3-+3S2-+6H+=Y-+3S↓+3H2O。请回答:
(1)YO3—中Y的化合价是_______。
(2)Y元素原子的最外层电子数是_______,它可能处于第_______族。
下图是元素周期表的前四周期的结构,请回答
| A |
|||||||||||||||||
| B |
C |
D |
|||||||||||||||
| E |
F |
G |
|||||||||||||||
| H |
|||||||||||||||||
⑴请写出各元素的元素符号:A、B、C、D、
⑵请写出C元素单质的结构式
⑶E、D两种元素可形成一种原子个数比为1:1的化合物M,请写出M的电子式,指出化合物M中的化学键类型。
⑷E、F、G三种元素的最高价氧化物对应的水化物可以两两反应,请写出反应的离子方程式:
E+F
E+G
F+G
⑸H的一种氢氧化物不稳定,很容易被氧气氧化,请写出该反应的化学方程式:
⑴一个确定的化学反应完成后的结果是吸收能量还是放出能量,决定于反应物的总能量与生成物的总能量的相对大小。若反应物的总能量(填“>”、“<”、“=”)生成物的总能量,该反应就放出能量;若反应物的总能量生成物的总能量,该反应就吸收能量。
⑵普通锌锰酸性干电池的内部结构如图所示,请回答
①该电池的负极材料为该电极反应为
②正极材料为,正极得到电子的氧化剂为
③电解质为
⑶化学反应速率通常用单位时间内反应物浓度的减少量或生成物浓度的增加量来表示。若时间用秒表示,则化学反应速率的单位是。
⑷在外界条件不变的情况下,一个可逆反应达到的最大限度是该反应达到状态。