某溶液中含有Fe2+和I -。为了氧化I -而不使Fe2+被氧化,试根据下列三个反应判断,可选用的氧化剂是( )
①2Fe3++2I-=2Fe2++I2
②2Fe2++Cl2=2Fe3++2Cl-
③2MnO4-+10Cl-+16H+=2Mn2++5Cl2↑+8H2O
| A.FeCl2 | B.KMnO4 | C.Cl2 | D.FeCl3 |
下列有关化学用语表示正确的是( )
A.CCl4的比例模型: |
B.对甲基苯酚的结构简式: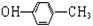 |
| C.乙醛的结构简式:C2H4O |
D.乙醇分子的比例模型: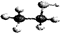 |
为了便于研究物质的性质,常常给物质进行分类。下列物质中,属于有机物的是( )
| A.MgC2 | B.NH4CN | C.CO(NH2)2 | D.Ca(HCO3)2 |
某有机物的结构简式是: 该物质不应有的化学性质是( )
该物质不应有的化学性质是( )
①可以燃烧 ②可以跟溴加成 ③可以将KMnO4酸性溶液还原 ④可以跟NaHCO3溶液反应 ⑤可以跟NaOH溶液反应 ⑥可以发生消去反应
| A.①③ | B.③⑥ | C.④⑥ | D.④⑤ |
由乙炔(C2H2)、苯(C6H6)、苯乙烯(C8H8)和乙醛(CH3CHO)组成的混合物中碳的质量分数为60%,则氢的质量分数为()
| A.5% | B.8.9% | C.17.8% | D.无法确定 |
下列表述与化学用语对应且正确的是()
A.CO2的比例模型: |
B.溴乙烷的消去反应:CH3CH2Br C2H4↑+HBr C2H4↑+HBr |
C. 的名称:2,3-二甲基-4-乙基己烷 的名称:2,3-二甲基-4-乙基己烷 |
| D.苯酚钠溶液中通入少量CO2的反应:2C6H5ONa+CO2+H2O—→2C6H5OH+Na2CO3 |