下列装置所示的实验中,能达到实验目的的是 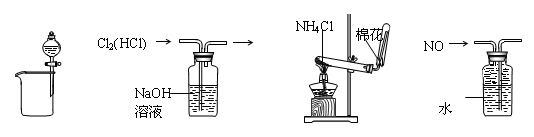
| A.分离碘和酒精 | B.除去Cl2中的HCl | C.实验室制氨气 | D.排水法收集NO |
下列离子反应方程式正确的是()
| A.澄清石灰水来吸收氯气:Cl2+OH—→Cl—+ClO—+H+ |
| B.将金属Na加入冷水中:2Na+2H2O→2Na++2OH—+H2↑ |
| C.向稀硝酸中加入少量铁粉:3Fe+8H++2NO3→3Fe2++2NO↑+4H2O |
| D.碳酸氢钙溶液中加入少量苛性钾溶液:Ca2++2HCO—3+2OH—→CaCO3↓+CO2-3+2H2O |
下列现象或反应的原理解释正确的是()
| 现象或反应 |
原理解释 |
|
| A |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔表面生成的氧化物具有高熔点 |
| B |
钠和氧气在加热条件下进行反应 |
该反应为吸热反应 |
| C |
碳酸钠和氢氧化钠溶液中滴加酚酞,溶液都呈红色 |
碳酸钠和氢氧化钠都是碱 |
| D |
铁制容器可用于盛装冷的浓硫酸 |
铁与浓硫酸不反应 |
设NA为阿伏加德罗常数,下列叙述中不正确的是()
| A.80g硝酸铵中含有氮原子数为2NA |
| B.在常温下,1mol氩气含有原子数为NA |
| C.32gCu与足量的硫蒸汽充分反应,电子转移总数为0.5NA |
| D.在标准状况下,11.2L SO3含分子数0.5NA |
下列各组离子在给定条件下,一定能大量共存的是()
| A.含有大量NO—3的水溶液中:NH+4、Fe2+、SO2-4、H+ |
| B.在pH=12的溶液中:ClO—、SO2-3、Na+、K+ |
| C.能与铝粉反应生成氢气的溶液中:Na+、Al3+、CH3COOO—、I— |
| D.含有大量HCO—3的澄清透明溶液中:K+、C6H5O—、Cr—、Na+ |
下列物质的性质(或性质递变规律)与键能有关的是()
| A.F2、Cl2、Br2、I2的熔、沸点逐渐升高 |
| B.NH3易液化 |
| C.HF、HC1、HBr、HI的热稳定性依次减弱 |
| D.H2S的熔沸点小于H2O的熔、沸点 |