某有机物A能与NaOH溶液反应,其分子中含有苯环,相对分子质量小于150,其中含碳的质量分数为70.6%,氢的质量分数为5.9%,其余为氧。
(1)A的分子式是 。
(2)若A能与NaHCO3溶液反应放出CO2气体,其结构可能有 种。
(3)若A与NaOH溶液在加热时才能较快反应,且1molA消耗1mol NaOH,则A的所有可能的结构简式是 。
(4)若A与NaOH溶液在加热时才能较快反应,且1mol A消耗2mol NaOH,则符合条件的A的结构可能有 种,其中不能发生银镜反应的物质的结构简式是: 。
已知:G、Q、R、T、X、Y、Z都是周期表中前四周期的元素,它们的核电荷数依次增大。G的简单阴离子最外层有2个电子,Q原子最外层电子数是内层电子数的两倍,X元素最外层电子数与最内层电子数相同;T2R的晶体类型是离子晶体,Y原子基态3p原子轨道上有2个未成对电子,其单质晶体类型属于原子晶体;在元素周期表中Z元素位于第10列。
回答下列问题:
⑴Z的核外电子排布式是。
⑵X以及与X左右相邻的两种元素,其第一电离能由小到大的顺序为。
⑶QR2分子中,Q原子采取杂化,写出与QR2互为等电子体的一种分子的化学式:。
⑷分子式为Q2G6R的物质有两种,其中一种易溶于水,原因是;T的氯化物的熔点比Y的氯化物的熔点高,原因是。
⑸据报道,由Q、X、Z三种元素形成的一种晶体具有超导性,其晶体结构如图所示。晶体中距每个X原子周围距离最近的Q原子有个。
(14分)乙醇汽油是被广泛使用的新型清洁燃料,工业生产乙醇的一种反应原理为:2CO(g)+4H2 (g)  CH3CH2OH(g)+H2O(g) △H=—256.1kJ·mol—1。
CH3CH2OH(g)+H2O(g) △H=—256.1kJ·mol—1。
已知:H2O(l)=H2O(g) △H=+44kJ·mol—1
CO(g)+H2O(g) CO2(g)+H2(g) △H=—41.2kJ·mol—1
CO2(g)+H2(g) △H=—41.2kJ·mol—1
⑴以CO2(g)与H2(g)为原料也可合成乙醇,其热化学方程式如下:
2CO2(g)+6H2(g)  CH3CH2OH(g)+3H2O(l) △H=。
CH3CH2OH(g)+3H2O(l) △H=。
⑵CH4和H2O(g)在催化剂表面发生反应CH4+H2O CO+3H2,该反应在不同温度下的化学平衡常数如下表:
CO+3H2,该反应在不同温度下的化学平衡常数如下表:
| 温度/℃ |
800 |
1000 |
1200 |
1400 |
| 平衡常数 |
0.45 |
1.92 |
276.5 |
1771.5 |
①该反应是_____反应(填“吸热”或“放热”);
②T℃时,向1L密闭容器中投入1molCH4和1mol H2O(g),平衡时c(CH4)=0.5mol·L—1,该温度下反应CH4+H2O CO+3H2的平衡常数K=。
CO+3H2的平衡常数K=。
⑶汽车使用乙醇汽油并不能减少NOx的排放,这使NOx的有效消除成为环保领域的重要课题。某研究小组在实验室以Ag-ZSM-5 为催化剂,测得NO转化为N2的转化率随温度变化情况如图。
①若不使用CO,温度超过775℃,发现NO的分解率降低,其可能的原因为;在n(NO)/n(CO)=1的条件下,应控制的最佳温度在左右。
②用CxHy(烃)催化还原NOx也可消除氮氧化物的污染。写出CH4与NO2发生反应的化学方程式:。
⑷乙醇-空气燃料电池中使用的电解质是搀杂了Y2O3的ZrO2晶体,它在高温下能传导O2—离子。该电池负极的电极反应式为。
(12分)某种铅酸蓄电池具有廉价、长寿命、大容量的特点,它使用的电解质是可溶性的甲基磺酸铅,电池的工作原理:
⑴放电时,正极的电极反应式为;充电时,Pb电极应该连接在外接电源的(填“正极”或“负极”)。
⑵工业用PbO2来制备KClO4的工业流程如下:
①写出NaClO3与PbO2反应的离子方程式:。
②工业上可以利用滤液Ⅰ与KNO3发生反应制备KClO4的原因是。
⑶PbO2会随温度升高逐步分解,称取23.9gPbO2,其受热分解过程中各物质的质量随温度的变化如右图所示。
若在某温度下测得剩余固体的质量为22.94g,则该温度下PbO2分解所得固体产物的组成为(写化学式),其物质的量之比为。
(15分)有机物G是一种食品香料,其香气强度为普通香料的3~4倍,有机物I的合成路线如下:
已知:
⑴该香料长期暴露于空气中易变质,其原因是。
⑵写出A中含氧官能团的名称:,由C到 D的反应类型为。
⑶有机物E的结构简式为。
⑷有机物G同时满足下列条件的同分异构体有种。
①与FeCl3溶液反应显紫色;
②可发生水解反应,其中一种水解产物能发生银镜反应;
③分子中有4种不同化学环境的氢。
⑸写出以 为原料制备
为原料制备 的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
的合成路线流程图(无机试剂任用)。合成路线流程图示例如下:
(12分)酸性条件下,锡在水溶液中有Sn2+、Sn4+两种主要存在形式。SnSO4是一种重要的硫酸盐,广泛应用于镀锡工业,其制备路线如下: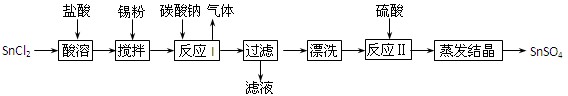
回答下列问题:
⑴SnCl2用盐酸而不用水直接溶解的原因是,加入Sn粉的作用是。
⑵反应I生成的沉淀为SnO,写出该反应的化学方程式:。
⑶检验沉淀已经“漂洗”干净的方法:。
⑷反应Ⅱ硫酸的作用之一是控制溶液的pH,若溶液中c(Sn2+)=1.0mol·L—1,则应控制溶液pH。已知:Ksp[Sn(OH)2]=1.0×10—26。
⑸酸性条件下,SnSO4还可以用作双氧水去除剂,试写出发生反应的离子方程式:
。