将NaCl溶液滴在一块光亮清洁的铁板表面上,一段时间后发现液滴覆盖的圆圈中心区(a)已被腐蚀而变暗,在液滴外沿形成棕色铁锈环(b),如图所示。导致该现象的主要原因是液滴之下氧气含量比边缘处少。下列说法正确的是( )‘
| A.液滴中的Cl- 由a区向b区迁移 |
| B.液滴边缘是正极区,发生的电极反应为:O2+2H2O+4e-=4OH- |
| C.液滴下的Fe因发生还原反应而被腐蚀,生成的Fe2+由a区向b区迁移,与b区的OH-形成Fe(OH)2,进一步氧化、脱水形成铁锈 |
| D.若改用嵌有一铜螺丝钉的铁板,在铜铁接触处滴加NaCl溶液,则负极发生的电极反应为:Cu-2e-=Cu2+ |
下列各项中表达正确的是()
A.NH3分子的电子式: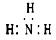 |
B.N2的结构式: N≡N |
| C.乙醇的结构简式C2H6O | D.CH4分子的比例模型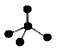 |
反应4NH3(g) + 5O2(g) 4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是()
4NO(g) + 6H2O(g)在5L密闭容器中进行,半分钟后,NO的物质的量增加了0.3mol,则表示此反应的速率正确的是()
| A.v (O2) = 0.01mol·(L·s) –1 | B.v (NO) =" 0.008mol·(L·s)" –1 |
| C.v (H2O) =" 0.003mol·(L·s)" –1 | D.v (NH3) =" 0.02mol·(L·s)" –1 |
下列关于下图所示装置的叙述,不正确的是()
| A.该装置是利用氧化还原反应将化学能转化成电能 |
| B.铁片质量逐渐减少,碳棒上有气泡产生 |
| C.电流由铁片经导线沿外电路流向碳棒 |
D.该装置总的化学反应为 |
2008年北京奥运会祥云火炬的燃料为丙烷(C3H8)。下列关于丙烷的说法不正确的是()
| A.属于烷烃 | B.分子中含有碳碳双键 |
| C.丙烷燃烧是放热反应 | D.丙烷充分燃烧生成二氧化碳和水 |
以氯乙烷为原料制取乙二酸(HOOC-COOH)的过程中,要依次经过下列步骤中的:
①与NaOH的水溶液共热 ②与NaOH的醇溶液共热 ③与浓硫酸共热到170℃ ④在催化剂存在情况下与氯气加成 ⑤在Cu或Ag存在的情况下与氧气共热 ⑥与新制的Cu(OH)2共热
| A.①③④②⑥ | B.①③④②⑤ | C.②④①⑤⑥ | D.②④①⑥⑤ |