在一定温度下,A、B能在溶液中发生反应A+B===C+D。
a.将0.2 mol/L A溶液和0.2 mol/L B溶液各20 mL混合
b.将0.5 mol/L A溶液和0.5 mol/L B溶液各50 mL混合
c.将1 mol/L A溶液和1 mol/L B溶液各10 mL混合,同时倒入30 mL蒸馏水
d.将1 mol/L A溶液20 mL和1.2 mol/L B溶液60 mL混合
反应开始时,反应速率由大到小的顺序是( )
A.d>b>c>a B.b>d>a>c
C.d>c>b>a D.b>c>d>a
下图为番茄电池,下列说法正确的是( ) 
| A.一段时间后,锌片质量会变小 | B.铜电极附近会出现蓝色 |
| C.番茄中的阴离子移向铜 | D.锌电极是该电池的正极 |
能说明Cl的非金属性比S强的事实有()
①常温下S为固体,而Cl2为气体 ②Cl2与H2混合,强光照射剧烈反应;而S与H2反应需较高温度 ③与Fe反应,Cl2生成FeCl3,而S生成FeS ④盐酸是强酸,而氢硫酸是弱酸 ⑤将Cl2通入氢硫酸中可置换出S
| A.①③⑤ | B.②③④ | C.②③⑤ | D.②④⑤ |
下列反应中,既属于氧化还原反应同时又是放热反应的是()
| A.酸碱中和反应 | B.Ba(OH)2.8H2O与NH4Cl |
| C.灼热的炭与CO2反应 | D.甲烷与O2的燃烧反应 |
化学概念在逻辑上存在如下图所示关系,对下列概念相互关系的说法正确的是()
| A.化学键与离子键(或共价键)属于包含关系 |
| B.化合物与电解质属于交叉关系 |
| C.单质与化合物属于交叉关系 |
| D.氧化还原反应与化合反应属于并列关系 |
下列有关化学用语表达不正确的是( )
| A.二氧化碳的结构式:O=C=O |
B.S2-的离子结构示意图: |
C.MgO的电子式:[Mg2+][∶ ∶]2- ∶]2- |
D.R2+离子核外有a个电子,b个中子,R原子表示为: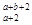 R R |