为进一步提高合成氨的生产能力,科研中最有开发价值的是 ( )。
| A.研制高温下活性较大的催化剂 |
| B.寻求氮气的新来源 |
| C.研制低温下活性较大的催化剂 |
| D.研制耐高温和高压的新材料建造合成塔 |
某一反应物的浓度是2mol· L-1,经过4min后,它的浓度变成1. 68 mol· L-1,则在这4min内它的平均反应速率为()
| A.0.2 mol· L-1 | B.0.1 mol· L-1 |
| C.0.04 mol· L-1 | D.0.08 mol· L-1 |
下列有机物在空气中燃烧,产生明亮火焰并带有浓烟的物质是()
| A.CH4 | B.CH2 ="CH2" | C. |
D.CH3CH2OH |
下列反应属于取代反应是
A.C3H8 + 5O2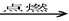 3CO2 +4H2O 3CO2 +4H2O |
B.CH4+C12 CH3C1+HCl CH3C1+HCl |
C.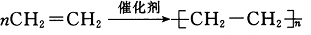 |
D. +3H2 +3H2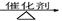  |
医院里检查患者是否患有糖尿病,是检测其尿液中的
| A.脂肪 | B.食盐 | C.蛋白质 | D.葡萄糖 |
下列有关甲烷性质的叙述,正确的是
| A.甲烷是一种无色,有臭味的气体 |
| B.甲烷易溶于水 |
| C.甲烷与氯气发生的化学反应类型属于取代反应 |
| D.甲烷是一种混合物 |