亚氯酸钠(NaClO2)是一种性能优良的漂白剂,但遇酸性溶液发生分解:5HClO2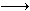 4ClO2↑+H++Cl-+2H2O。向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反应缓慢,稍后一段时间产生气体速度较快,其原因可能是……( )。
4ClO2↑+H++Cl-+2H2O。向亚氯酸钠溶液中加入盐酸,反应剧烈。若将盐酸改为硫酸,开始时反应缓慢,稍后一段时间产生气体速度较快,其原因可能是……( )。
| A.逸出ClO2使生成物浓度降低 | B.酸使亚氯酸的氧化性增强 |
| C.溶液中的H+起催化作用 | D.溶液中的Cl-起催化作用 |
对于反应A+3B = 2C+D来说,下列反应速率中最快的是
A.v(A)=0.3mol·L-1·min-1 B.v(B)=0.01mol·L-1·s-1
C.v(C)=0.5mol·L-1·min-1 D.v(D)=0.006mol·L-1·s-1
下图为某兴趣小组制作的番茄电池,下列说法正确的是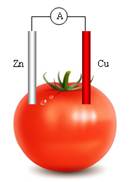
| A.电流由锌通过导线流向铜 |
| B.该装置将电能转化为化学能 |
| C.锌电极发生氧化反应 |
| D.铜电极的质量会不断减少 |
化学与生活、社会密切相关。下列做法正确的是
| A.城市生活垃圾应分类处理,废旧电池回收后集中掩埋,废弃的塑料焚烧处理 |
| B.若将原来燃烧液化石油气的灶具改成烧天然气,应增大空气进气量和减少天然气进入量 |
| C.鉴别棉纺线与羊毛线可用灼烧法鉴别 |
| D.糖尿病人可用氢氧化铜悬浊液检验其新鲜尿样中蔗糖含量的高低 |
下列关于卤族元素由上到下性质递变的叙述,正确的是
①元素的非金属性增强②单质的颜色加深③气态氢化物的稳定性增强
④单质的沸点升高⑤阴离子的还原性增强
| A.①②③ | B.②③④ |
| C.②④⑤ | D.①④⑤ |
下列各组给定原子序数的元素,不能形成原子数之比为1:1稳定化合物的是
| A.11和17 | B.1和8 |
| C.1和6 | D.6和12 |