结构决定性质,性质决定用途;已知X、Y、Z、W是元素周期表中短周期中的四种非金属元素,它们的原子序数依次增大,X元素的原子形成的阳离子就是一个质子,Z、W在元素周期表中处于相邻的位置,Z的单质在常温下均为无色气体,W原子的最外层电子排布是nSn npn+2,Y原子的最外层电子数是内层电子数的2倍。试回答:
(1)写出W元素的元素符号和该原子基态的电子排布式:__ _____
(2)写出Z元素的原子结构示意图和该原子基态的电子排布图: _ _____
(3)X单质和Z单质在一定条件下反应生成化合物E,则E的电子式是: 。E可以进行喷泉实验的主要原因是: 。
(4)仅由X、Z、W三种元素组成的某种盐是一种速效肥料,但长期施用会使土壤酸化,有关的离子反应方程式为___________ __________________
(5)这四种元素可组成原子个数比为5∶1∶1∶3的化合物(按X、Y、Z、W的顺序)为(写名称) ,该化合物的浓溶液与足量NaOH热浓溶液反应的离子方程式为:____________ __ __
PTT纤维综合了尼龙的柔软性、腈纶的蓬松性、涤纶的抗污性,加上本身固有的弹性,以及能常温染色等特点,把各种纤维的优良性能集于一身,从而成为当前国际上最新开发的热门高分子新材料之一。下面是制备PTT的一种线路: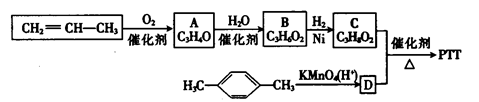
已知:①A、B、C均为链状化合物,A能发生银镜反应,B结构中含有两种含氧官能团;
②C的核磁共振氢谱表明其有三种不同化学环境的氢,且三种氢原子的个数之比为1 :2 : 1;
③1 mol D与足量碳酸氢钠溶液反应可生成2 mol CO2。
(1)B中所含官能团的名称是__________,A的结构简式是_________。
(2)C的系统名称是________,写出与C含有相同官能团的C的一种同分异构体的结构简式:__________________。
(3)写出下列反应的反应类型;A→B__________,C+D→PTT__________。
(4)C与D反应生成PTT的化学方程式是____________________________________。
香豆素是一种用途广泛的香料,可以利用乙醇和B(分子式为C7H6O2)通过以下途径合成。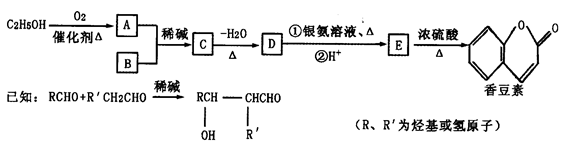
(1)D→E中①的反应类型为________________________________;
C中含氧官能团的名称为_________________________________。
(2)有关香豆素的说法正确的是___________________________(填字母)。
a.易溶于水和酒精中
b.长期放置香豆素,容易氧化变质
c.能发生加成反应,不能发生取代反应
d.1mol香豆素可与2molNaOH反应
(3)B有多种同分异构体,其中苯环上只有一个侧链的同分异构体的结构简式是________________(写一种即可)。
(4)乙醇生成A的化学方程式为__________________________。
X、Y、Z、Q、W为按原子序数由小到大排列的五种短周期元素,已知:
①x元素与Q处于同一主族,其原子价电子排布式都为ns2np2,且x原子半径小于Q的原子半径;
②Y元素是地壳中含量最多的元素;w元素的电负性略小于Y元素;在w原子的电子排布中,P轨道上只有1个未成对电子;
③Z元素的电离能数据见下表(kJ·mol-1)
| I1 |
I2 |
I3 |
I4 |
… |
| 496 |
4562 |
6912 |
9540 |
… |
(1)XY2分子空间构型为____________________________。QX的晶体结构与金刚石的相似,其中X原子的杂化方式为_______________,微粒间存在的作用力是____________。
(2)晶体ZW的熔点比晶体XW4明显高的原因是______________。
(3)氧化物MO的电子总数与QX的相等,则M为_____(填元素符号)。MO是优良的耐高温材料,其晶体结构与ZW晶体相似。MO的熔点比CaO的高,其原因是___________________________________。
已知:醛分子间可相互发生缩合反应,这是使碳链增长的重要方式之一,例如:
R-CHO+CH3CHO R-CH=CH-CHO+H2O
R-CH=CH-CHO+H2O
有机物E可分别由有机物A和C通过下列两种方法制备: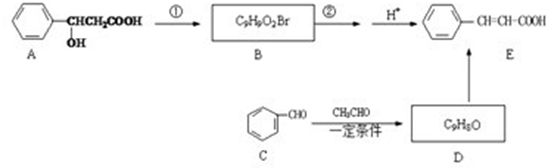
(1)有机物D的结构简式为,反应②的反应类型是:。
(2)写出B与NaOH水溶液共热的化学方程式。
(3)E有多种同分异构体,其中与E具有相同官能团,且属于芳香族化合物的物质有种。
(4)乙基香草醛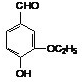 (是有机物A的同分异构体),下列说法错误的是
(是有机物A的同分异构体),下列说法错误的是
a.乙基香草醛能与NaHCO3溶液反应
b.乙基香草醛能与浓溴水发生取代反应
c.lmol乙基香草醛最多能与3molH2发生加成反应
d.乙基香草醛和有机物A能用FeCl3溶液来鉴别
A、B、C都是元素周期表中的短周期元素,它们的核电荷数依次增大。第2周期元素A原子的核外成对电子数是未成对电子数的2倍,B原子的最外层p轨道的电子为半充满结构,C是地壳中含量最多的元素。D是第四周期元素,其原子核外最外层电子数与氢原子相同,其余各层电子均充满。请用对应的元素符号或化学式填空:
(1)A、B、C的第一电离能由小到大的顺序为。
(2)A的最高价含氧酸根离子中其中心原子采取杂化。
(3)与A、B形成的阴离子(AB-)互为等电子体的分子有。
(4)基态D原子的核外电子排布式为,下图是金属Ca和D所形成的某种合金的晶胞结构示意图,则该合金中Ca和D的原子个数比为。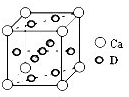
(5)向D的高价态硫酸盐溶液中逐滴滴加B的氢化物水溶液至过量,先出现沉淀,最后沉淀溶解形成溶液。写出此沉淀溶解的离子方程式:____。