在2L的密闭容器中,充入1molSO2和1molO2,在一定条件下发生反应:2SO2+O2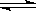 2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
2SO3,当反应进行了10s时,测得SO2的物质的量为0.6mol,求:
(1)用SO2表示该化学反应速率为多少?
(2)若改用O2表示化学反应速率又为多少?
(3)若要提高反应速率你认为可采取的合理措施有哪些?
有NaCl和KCl的混合物25g,溶于水形成溶液,加入1000g 7.14%的AgNO3溶液,充分反应后滤出沉淀,再向混合物加入100g Cu片,过一段时间取出(反应完全),洗涤干燥称其质量为101.52g,求原混合物中NaCl和KCl的物质的量各为多少?
用含杂质(杂质不与酸作用,也不溶于水)的铁10克与50克稀硫酸完全反应后,滤去杂质,所得液体质量为55.4克,求此铁的纯度。
将12克CO和CO2的混合气体通过足量灼热的氧化铜后,得到气体的总质量为18克,求原混合气体中CO的质量分数。
将质量为100克的铁棒插入硫酸铜溶液中,过一会儿取出,烘干,称量,棒的质量变为100.8克。求有多少克铁参加了反应。
某气体混合物含有氢气,二氧化碳和45%(体积)的氮气。它对氢气的相对密度是12.2,试求氢气和二氧化碳在混合气体中各自的体积百分含量