化学兴趣小组对某品牌牙膏中碳酸钙含量进行以下探究。该牙膏摩擦剂主要由碳酸钙、氢氧化铝组成,其他成分遇到盐酸时无气体生成。现利用下图所示装置(图中夹持仪器略去)进行实验,充分反应后,测定B中生成的BaCO3沉淀质量,以确定碳酸钙的质量分数。请回答下列问题。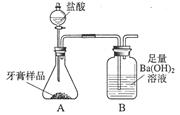
(1)装置A中牙膏样品放置在 (填仪器名称)中,盐酸放置在装置 (填仪器名称)中,A中至少发生 (填数字)个反应,写出其中一个反应的化学方程式 。
(2)若测定值比实际值小,可能的原因有 。(填字母)
a.装置A中水蒸气、HCl等进入装置B中 b.装置A中CO2未完全进入装置B
c.CO2气流速度太快导致Ba(OH)2未完全吸收 d.盐酸未滴加过量
(3)为减少误差,现采取以下一些措施:
①在A、B之间增加一个装有 (填化学式)溶液的洗气瓶,它的作用是 _;
②将装置B中的长导管下方增加一个带孔球泡,可以提高 ;
③在装置B的后面再增加一个装有 (填药品名称或化学式)固体的干燥管,目的是 。
(4)准确称取三份各16.00 g的样品,进行测定,测得BaCO3质量分别为3.96 g、3.92 g、3.94 g。请计算样品中碳酸钙的质量分数。 。(写出计算过程,4分)
(5)某同学利用上述方法测定牙膏中钙元素的质量分数。小李同学认为即使排除实验仪器和操作的影响,上述测定的结果仍有可能偏小,理由是 。
某化学兴趣小组按照课本实验方法(如下图),做木炭与氧化铜反应的实验时,发现很难观察到紫红色铜的生成,却往往有暗红色固体出现。他们决定对这个实验进行探究和改进。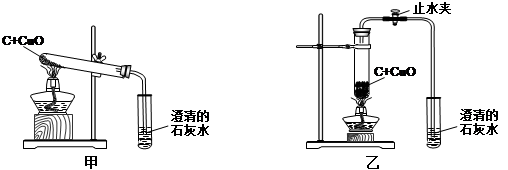
【提出问题】暗红色的固体是什么?如何选择合适条件,使木炭还原氧化铜的实验现象更明显?
【查阅资料】铜有+1和+2两种化合价,通常情况下,氧的化合价为-2,碳的化合价为+4或-4。
【猜想与假设】
(1)同学们认为这种暗红色固体可能是一种化合物,并猜测它的化学式为。
(2)同学们还认为,通过改变反应物的状态、质量比,以及反应装置,可以使该实验现象更加明显,减少出现暗红色固体的情况。
【分析与交流】
(1)小吴建议用超细炭粉与氧化铜粉末进行实验。你认为这样建议的原理是;
反应的化学方程式为:。
(2)小周建议用图乙装置替代甲装置。与甲相比较,乙装置中将试管直立放置的作用是
。
【实验与结论】
同学们决定按改进后的方案进行实验,他们在检验了乙装置的后,往试管中加入已干燥的药品并开始加热,当看到澄清的石灰水刚出现浑浊时,(填“可以”或“不能”)确定氧化铜和炭粉已经开始反应。
不久,即可看到试管底部变红热,停止加热后,仍能看到红热现象,并沿试管底部自下而上蔓延,这个现象说明该反应是(填“吸”或“放”)热反应。
待产物冷却后,同学们终于找到了期待已久的紫红色铜珠,实验获得了圆满成功。
某兴趣小组同学对实验室制取氧气的条件进行如下探究实验.
(1)为探究催化剂的种类对氯酸钾分解速度的影响,甲设计以下对比试验:
I.将3.0gKClO3与1.0gMnO2均匀混合加热
II.将xgKClO3与1.0gCuO均匀混合加热
在相同温度下,比较两组实验产生O2的快慢.
①II中x的值为 .
②若要证明CuO能作为KClO3分解的催化剂,则还要证明在化学反应前后CuO的 和 都不改变.
(2)乙探究了影响双氧水分解速度的某种因素,实验数据记录如表:
| 双氧水的质量 |
双氧水的浓度 |
MnO2的质量 |
相同时间内产生O2的体积 |
| I |
50.0g |
1% |
0.1g |
9mL |
| II |
50.0g |
2% |
0.1g |
16mL |
| III |
50.0g |
4% |
0.1g |
31mL |
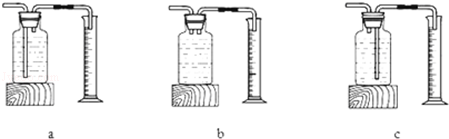
①若用上述装置测生成氧气的体积,则用图 (填“a”“b”或“c”)
②实验结论:在相同条件下, ,双氧水分解得快.
在化学实验室里,酒精是最常用到的一种燃料,其化学式是C2H6O。小明为了证明酒精中含有碳、氢元素,设计并完成如下实验方案。请你帮他完成下面的实验报告。
【实验目的】:证明酒精中含有碳、氢元素。
【实验用品】:酒精灯、火柴、洁净干燥的小烧杯、澄清石灰水
【实验过程及结论】
| 实验步骤 |
实验现象 |
实验结论 |
步骤一:点燃酒精灯,将洁净干燥的小烧杯罩在火焰上方 |
烧杯内壁 有生成; |
证明酒精中含有元素 |
步骤二:迅速取下烧杯,并加入少量,振荡; |
证明酒精中含有碳元素 |
某学校科学兴趣小组在研究“带火星木条复燃与氧气体积分数的关系”的课题中,采取了以下实验步骤:①取5只250mL集气瓶,向5只集气瓶中分别装入25mL、50mL、75mL、100mL、125mL的水,并用毛玻璃片盖住,依次编号为1、2、3、4、5.②用分解过氧化氢(H2O2)的方法制取氧气,用制取的氧气通过排水法将上述1﹣5号瓶中的水排去.③将带火星的木条依次插入1﹣5号瓶中,把观察到的现象和计算数据,填入下表.
| 集气瓶标号 |
1 |
2 |
3 |
4 |
5 |
| 集气瓶中收集氧气的体积 |
25mL |
50mL |
75mL |
100mL |
125mL |
| 带火星木条的状况 |
微亮 |
亮 |
很亮 |
复燃 |
复燃 |
试回答下列问题:
(1)从观察到的现象知,使带火星的木条复燃所需氧气的最小体积分数介于 号瓶至 号瓶之间]
(2)实验室中采用分解过氧化氢的方法制取氧气,其反应的文字表达式为 ,反应类型属于
(3)根据以上实验事实,下列说法中正确的是
A.只有在纯氧中才能使带火星的木条复燃
B.集气瓶中氧气的体积分数≥52.6%时,带火星的木条就能复燃
C.只要有氧气存在就可使带火星的木条复燃
(4)当4号瓶收集氧气为100mL时,那么瓶中实际氧气所占的体积分数为 %,上述实验表明:物质燃烧的程度与氧气的浓度有关,氧气浓度越大,燃烧越剧烈.(如你能再设计一个实验来说明此问题可奖励2分).
如图1是小红按课本进行的一个化学实验,在进行实验时我们都闻到一股难闻的刺激性气味,小明于是对原实验进行了重新设计,如图2,实验装置如下: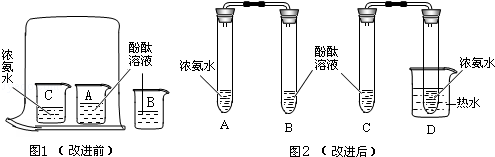
实验操作
a.向盛有20mL蒸馏水的烧杯中滴入3﹣4滴无色酚酞溶液,搅拌均匀,观察溶液颜色.
b.取少量上述溶液于试管中,向其中慢慢滴加浓氨水,观察现象.
c.在B、C试管内分别倒入5mL烧杯中的酚酞溶液(烧杯中剩余的酚酞溶液用于实验中作比较).然后在一空烧杯中倒入适量的热水备用.另在A、D试管中分别倒入2mL浓氨水,立即用带橡皮塞的导管按实验如图2连接好,并将D试管放置在热水中,观察几分钟,
请回答:
(1)进行操作a的实验目的是 ;
(2)操作c观察到的现象是 ;
(3)由此可以得到的实验结论是① ② ;
(4)对比改进前的实验还有一个优点是 .