已知25℃时弱电解质电离平衡常数:
Ka(CH3COOH) l.8 xl0-5,Ka(HSCN) 0.13
(1)将20mL,0.10mol/L CH3COOH溶液和20mL,0.10mol/L的HSCN溶液分别与0.10mol/L的NaHCO3溶液反应,实验测得产生CO2气体体积(V)与时间t的关系如图。
反应开始时,两种溶液产生CO2的速率明显不同的原因是 ;
反应结束后所得溶液中c(SCN-)____ c(CH3COO-)(填“>”,“=”或“<”)。
(2)2.0×l0-3mol/L的氢氟酸水溶液中,调节溶液pH(忽略调节时体积变化),测得平衡体系中c(F-),c(HF)与溶液pH的关系如下图。
则25℃时,HF电离平衡常数为:(列式求值)Ka(HF)=
(3)难溶物质CaF2溶度积常数为:Ksp= 1.5×10-10,将4.0×10-3mol/L HF溶液与4.0×l0-4 mol/L的CaCl2溶液等体积混合,调节溶液pH =4(忽略调节时溶液体积变化),试分析混合后是否有沉淀生成?____ (填“有”或“没有”),筒述理由: 。
2012年12月1日美国航天局又一次对月球进行了撞击,撞击激起了1万多米高的尘土,在尘土中含有大量的月海玄武岩。月海玄武岩中的铁钛矿不仅是铁、钛和氧的主要资源,而且钛铁矿与氢气反应能产生水 (FeTiO3+H2―→Fe+TiO2+H2O),生成的TiO2经下列转化可制取重要金属Ti:TiO2―→TiCl4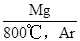 Ti据此回答下列问题:
Ti据此回答下列问题:
(1)在钛铁矿与氢气反应中,还原产物是________。
(2)反应TiCl4+2Mg 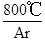 2MgCl2+Ti在Ar气氛围中进行的理由是______。
2MgCl2+Ti在Ar气氛围中进行的理由是______。
(3)TiO2与氯气反应生成TiCl4和另一种单质气体的化学方程式为________。
有A、B、C、D、E和F六瓶无色溶液,他们都是中学化学中常用的无机试剂。纯E为无色油状液体;B、C、D和F是盐溶液,且它们的阴离子均不同。现进行如下实验:
①A有刺激性气味,用蘸有浓盐酸的玻璃棒接近A时产生白色烟雾;
②将A分别加入其他五种溶液中,只有D、F中有沉淀产生;继续加入过量A时,D中沉淀无变化;F中沉淀完全溶解;
③将B分别加入C、D、E、F中,C、D、F中产生沉淀,E中有无色、无味气体逸出;
④将C分别加入D、E、F中,均有沉淀生成,再加入稀HNO3,沉淀均不溶。
根据上述实验信息,请回答下列问题:
(1)能确定的溶液是(写出溶液标号与相应溶质的化学式):
_________________________________________________________________;
(2)不能确定的溶液,写出其标号、溶质可能的化学式及进一步鉴别的方法:_________________________________________________________________。
今有一混合物的水溶液,只可能含有以下离子中的若干种:K+、Al3+、Fe3+、Mg2+、Ba2+、NH4+、Cl-、CO32-、SO42-,现取三份100 mL溶液进行如下实验:
①第一份加入AgNO3溶液有沉淀产生。
②第二份加过量NaOH溶液加热后,只收集到气体0.02 mol,无沉淀生成,同时得到溶液甲。
③在甲溶液中通入过量CO2,生成白色沉淀,沉淀经过滤、洗涤、灼烧,质量为1.02 g。
④第三份加足量BaCl2溶液后,得白色沉淀,沉淀经足量盐酸洗涤、干燥后,质量为11.65 g。
根据上述实验回答:
(1)一定不存在的离子是________________,不能确定是否存在的离子是________。
(2)试确定溶液中肯定存在的阴离子及其浓度(可不填满):
离子符号________,浓度__________________________________________;
离子符号________,浓度__________________________________________;
离子符号________,浓度_________________________________________。
(3)试确定K+是否存在________(填“是”或“否”),判断的理由是________________________________________________________________________。
用数轴表示化学知识,并按某种共性对化学物质进行分类,有简明易记的效果。例如,根据碳素钢的含碳量,将其分为低碳钢、中碳钢、高碳钢,利用数轴分类法可将其表示为: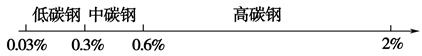
根据这一分类方法请回答:
(1)将pH与溶液酸碱性的关系粗略地表示在如下数轴上:
(2)某化学兴趣小组欲研究H2SO4、KCl、NaCl、Na2CO3、Na2SO3、NaOH六种物质的性质,对于如何研究,他们设计了两种研究方案:
方案Ⅰ:将它们按照酸、碱、盐分类,然后分别溶于水得到溶液,进行实验。
方法Ⅱ:将它们按照钠盐、钾盐和其他化合物分类,然后分别溶于水得到溶液,进行实验。
①根据方案Ⅰ进行分类时,经实验测得KCl、NaCl溶液的pH等于7;H2SO4溶液的pH小于7;Na2SO3、Na2CO3、NaOH溶液的pH大于7。由此有的同学按分类法思想把Na2SO3、Na2CO3与NaOH都划分为碱类是否合理?为什么?_____________________________。
②在方案Ⅰ中,某同学发现盐类物质中的KCl、NaCl在与其他物质混合时现象相同,无法区分,请设计一种简单的方法区分这两种物质_____________________________。
③在方案Ⅱ中,三种钠盐用其他物质中的________可加以区分,有关反应的化学方程式分别为_____________________________________________________________________。
④该兴趣小组中的一位同学认为,还可以根据是否含有钠元素将上述六种物质分为Na2SO3、Na2CO3、NaCl、NaOH和H2SO4、KCl两类。在用H2SO4鉴别四种含钠元素的物质时,Na2SO3和Na2CO3很容易得到了区分,但鉴别NaCl和NaOH时却陷入了困境,请设计一个实验来解决这一难题:__________________________________________。
用18mol/L的浓硫酸配制100mL 1mol/L硫酸,
①量取浓硫酸的体积应为mL,用量筒量取浓硫酸缓缓倒入盛水的烧杯中后,(填“应该”或“不应”)用少量蒸馏水洗涤量筒2~3次并将洗涤溶液也倒入烧杯中。
②若实验仪器有:A.100mL量筒 B.托盘天平 C. 玻璃棒 D. 50mL容量瓶
E. 10mL量筒F. 胶头滴管 G. 50mL烧杯 H. 100mL容量瓶实验时应选用的仪器有(填入编号,下同)。
③定容时,若俯视液面,则所配溶液浓度(填“偏高”、 “偏低” 或“无影响”)
若不小心加水超过了容量瓶刻度线,应。
A.用胶头滴管将多余溶液吸出 B.加热容量瓶使水挥发 C.重新配制