化学式为C8H10的芳香烃,苯环上的一硝基(—NO2是一种官能团)取代物只有一种,该芳香烃的名称是( )
| A.乙苯 | B.邻二甲苯 |
| C.间二甲苯 | D.对二甲苯 |
下列有机物的名称肯定错误的是( )
| A.2甲基1丁烯 |
| B.2,2二甲基丙烷 |
| C.5,5二甲基3己烯 |
| D.4甲基2戊炔 |
根据有机化合物的命名原则,下列命名正确的是( )
A.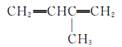 3甲基1,3丁二烯 3甲基1,3丁二烯 |
B. 2羟基丁烷 2羟基丁烷 |
| C.CH3CH(C2H5)CH2CH2CH3 2乙基戊烷 |
| D.CH3CH(NH2)CH2COOH 3氨基丁酸 |
某烯烃的结构简式为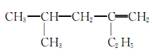 ,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯。下列对四位同学的命名判断正确的是( )
,甲、乙、丙、丁四位同学分别将其命名为:2甲基4乙基1戊烯、2异丁基1丁烯、5甲基3己烯、4甲基2乙基1戊烯。下列对四位同学的命名判断正确的是( )
| A.甲的命名主链选择是错误的 |
| B.乙的命名正确 |
| C.丙的命名主链选择是正确的 |
| D.丁的命名正确 |
有机物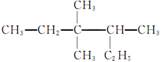 的正确命名为( )
的正确命名为( )
| A.2乙基3,3二甲基4乙基戊烷 |
| B.3,3二甲基4乙基戊烷 |
| C.3,3,4三甲基己烷 |
| D.2,3,3三甲基己烷 |