氢氧燃料电池已用于航天飞机。以30% KOH溶液为电解质溶液的这种电池在使用时的电极反应如下:负极:2H2+4OH--4e-===4H2O;正极:O2+2H2O+4e-===4OH-;据此作出判断,下列说法中错误的是( )
| A.H2在负极发生氧化反应 | B.供电时的总反应为2H2+O2===2H2O |
| C.产物为无污染的水,属于环境友好电池 | D.燃料电池的能量转化率可达100% |
在80g密度为dg/cm3的硫酸铁溶液中,含有2.8gFe3+离子,则此溶液中SO42-的物质的量浓度为()
A.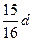 |
B.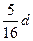 |
C.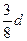 |
D.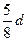 |
NA为阿伏加德罗常数,下列叙述正确的是()
| A.80g硝酸铵中含有氮原子数为NA |
| B.1molC3H8分子中共价键总数为11NA |
| C.5.6g铁与足量盐酸反应转移的电子数为0.3NA |
| D.0.1molN5+离子中所含的电子数为3.4NA |
下列物质中,与0.3moLH2O含相同氢原子数的物质是()
| A.18.9gHNO3 | B.3.612×1023个HNO3分子 |
| C.0.1moLH3PO4 | D.4.48LCH4(标准状况) |
下列变化中,必须加入氧化剂才能发生的是()
| A.Cl2→HCl | B.NaCl→Cl2 | C.Fe2+→Fe3+ | D.NaHCO3→CO2 |
下列叙述正确的是()
| A.盐酸和食醋既是化合物又是酸 |
| B.凡是生成两种或两种以上物质的反应都是分解反应 |
| C.氯化钠和HCl溶于水都发生电离,克服粒子间作用力的类型相同 |
| D.一种元素可能有多种氧化物,且一种化合价可能不止对应一种氧化物 |