钢铁的生产和使用是人类文明和生活进步的一个重要标志。
(1)金属制品中的镀锡铁皮(马口铁)和镀锌铁皮(白铁皮)镀层部分破坏后,在潮湿的环境中, (填“马口铁”或“白铁皮”)更易锈蚀。
(2)人们常用氧化铁进行铝热反应来焊接钢轨,写出该铝热反应的化学方程式:
。
(3)炒过菜的铁锅未及时洗净(残液中含NaCl),第二天便会因腐蚀出现红褐色锈斑。
①铁锅所发生的腐蚀主要是 腐蚀。
②铁锅锈蚀的正极反应式为 。
(4)为防止轮船的船体在海水中腐蚀,一般在轮船身上装有一定数量的 (填“锌”或“铜”)块。
(5)工业炼铁原理的主要化学反应方程式(即赤铁矿生成铁)为 。
A、B、C、D、E、F为元素周期表前四周期的元素,原子序数依次增大,A元素的单质是空气的主要成分,B原子核外p轨道上有1对成对电子,C与B同主族,D元素的价电子数是其余电子数的一半,E与D同族,F与A同主族,回答下列问题:
(1)D、E所在周期原子最外层电子数为1的元素有____________种。
(2)A、B、C第一电离能由大到小的顺序为______________(用元素符号表示);
(3)B与C形成的二元化合物中,属于非极性分子的是________(填化学式);该分子中心原子的杂化类型为____________;
(4)E和F形成的一种化合物的晶体结构如图所示,则该化合物的化学式为______________;F的配位数为____________;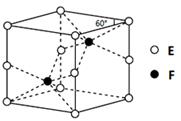
(5)D的离子可以形成多种配合物,由Dn+、Br-、C的最高价含氧酸根和A的简单氢化物形成的1:1:1:5的某配合物,向该配合物的溶液中滴加AgNO3溶液产生淡黄色沉淀,滴加BaCl2溶液无现象,则该配合物的化学式为________;n值为________;Dn+的基态电子排布式为________;
Ⅰ.图1是某压强下工业合成氨生产过程中,N2与H2按体积比为1:3投料时,反应混合物中氨的体积分数随温度的变化曲线,其中一条是经过一定时间反应后的曲线,另一条是平衡时的曲线。
(1)图中表示该反应的平衡曲线的是__________(填“Ⅰ”或“Ⅱ”);由图中曲线变化趋势可推知工业合成氨的反应是___________(填“吸热”或“放热”)反应。
(2)图中a点,容器内气体n(N2):n(NH3)= ____________,图中b点,v(正)_________v(逆)(填“>”、“=”或“<”)。
Ⅱ.以工业合成氨为原料,进一步合成尿素的反应原理为:2NH3(g)+CO2(g) CO(NH2)2(l)+H2O(g)
CO(NH2)2(l)+H2O(g)
工业生产时,需要原料气带有水蒸汽,图2中曲线I、Ⅱ、Ⅲ表示在不同水碳比[n(H2O)/n(CO2)]时,CO2的转化率与氨碳比[n(NH3)/n(CO2)]之间的关系。
(1)写出该反应的化学平衡常数表达式____________________
(2)曲线Ⅰ、Ⅱ、Ⅲ对应的水碳比最大的是_________,判断依据是_______________
(3)测得B点氨的转化率为40%,则x1=__________。
某化工厂以软锰矿、闪锌矿(主要成分为MnO2、ZnS,还含有少量的FeS、CuS、Al2O3等物质)为原料制取Zn和MnO2。
(1)在一定条件下,将这两种矿粉在硫酸溶液中相互作用,可得到含有Mn2+、Fe3+、Cu2+、Al3+、Zn2+的酸性溶液,其中发生的主要反应之一如下,请配平此反应方程式:_____MnO2+_____FeS+_____H2SO4=_____MnSO4+_____Fe2(SO4)3+_____S+_____H2O
(2)将所得溶液按以下的工业流程(如图I)进行操作处理得溶液(IV),电解溶液(IV)即得MnO2和Zn.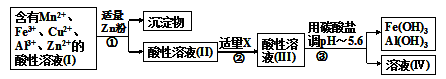 图(Ⅰ)
图(Ⅰ)
a.操作①中加Zn粉后发生反应的离子方程式为_________________;
b.操作②中加入适量X的作用是_________________;
c.工业上用惰性电极电解溶液(IV)获得产品,请写出电解过程中的阳极反应式_________________;
(3)为了从上述流程中产生的Fe(OH)3、Al(OH)3沉淀混合物中回收Al(OH)3,工厂设计了如下的有关流程如图(Ⅱ)。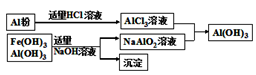 图(Ⅱ)
图(Ⅱ)
a.AlCl3溶液和NaAlO2溶液反应生成Al(OH)3的离子方程式为_________________;
b.若得到n molAl(OH)3,则理论上消耗的NaOH和HCl的物质的量分别为___________、__________;
X、Y、Z、W为四种短周期元素,其中Y元素原子核外最外层电子数是其电子层数的3倍,它们在周期表中的相对位置如下图所示:
| X |
Y |
|
| Z |
W |
请回答下列问题:
(1)W位于周期表中第__________周期,第________族;
(2)X可形成双原子分子,其分子的电子式是___________;Y和氢元素形成的10电子微粒中常见的+1价阳离子为_________(填化学式,下同);Z和氢元素形成的18电子微粒中常见的-1价阴离子为__________;
(3)工业上将干燥的W单质通入熔融的Z单质中可制得化合物Z2W2,该物质可与水反应生成一种能使品红溶液褪色的气体,0.2mol该物质参加反应时转移0.3mol电子,其中只有一种元素化合价发生改变,写出Z2W2与水反应的化学方程式______________________。
(4)在一定条件下,由元素Y和Z组成的一种气态化合物可发生催化氧化反应,反应达平衡进有三种气态物质共存,已知每转移4mol电子放热190.0kJ,该反应的热化学方程式是_____________。
碳元素在生产生活中具有非常重要的作用,在新物质的制备中也发挥了举足轻重的作用。碳元素的单质有多种形式,下图依次是C60、石墨和金刚石的结构图: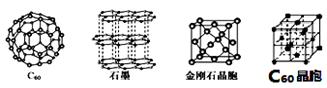
(1)与碳同周期,且基态原子的核外未成对电子数与碳相等的元素,其基态原子的电子排布式为 。
(2)金刚石、石墨、C60、碳纳米管等都是碳元素的单质形式,它们互为 。
(3)金刚石、石墨烯(指单层石墨)中碳原子的杂化形式分别为 、 。常温条件下丙烯是气态,而相对分子质量比丙烯小的甲醇,常温条件下却呈液态,出现这种现象的原因 。
(4)C60属于 晶体(,C60晶体内含有的微粒间作用有 。
(5)金刚石晶胞含有 个碳原子。若碳原子半径为r,金刚石晶胞的边长为a,根据硬球接触模型,则r= a,列式表示碳原子在晶胞中的空间占有率 (不要求计算结果)。