绿色化学的着眼点是使污染消灭在生产的源头,使整个合成过程和生产工艺对环境友好。其中合成方法应设计成能将所有的起始物质嵌入最终产物中,不产生任何废弃物,这时的原子利用率为100%。下列反应原子利用率可以达到100%的是 ( )
| A.加成反应 | B.消去反应 |
| C.取代反应 | D.醇的催化氧化反应 |
下列工业生产过程中涉及到反应热再利用的是
| A.接触法制硫酸 | B.联合法制纯碱 |
| C.铁矿石炼铁 | D.石油的裂化和裂解 |
下图是用于制取、收集并吸收多余气体的装置,下列方案正确的是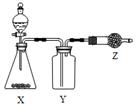
| 选项 |
X |
Y |
Z |
| A |
食盐、浓硫酸 |
HCl |
碱石灰 |
| B |
CaO、浓氨水 |
NH3 |
无水CaCl2 |
| C |
Cu、浓硝酸 |
NO2 |
碱石灰 |
| D |
电石、食盐水 |
C2H2 |
含溴水的棉花 |
将燃着的H2S不断通入盛有一定量O2的集气瓶中。当火焰熄灭后继续通入H2S,发生的主要反应是
| A.2H2S+O2→2S+2H2O | B.2H2S+3O2→2SO2+2H2O |
| C.2H2S+SO2→3S+2H2O | D.2SO2+O2→2SO3 |
液态氨中可电离出极少量的NH2-和NH4+。下列说法正确的是
| A.NH3属于离子化合物 | B.常温下,液氨的电离平衡常数为10-14 |
| C.液态氨与氨水的组成相同 | D.液氨中的微粒含相同的电子数 |
常温下,往饱和石灰水中加入一定量的生石灰,一段时间后恢复到原温度,以下叙述错误的是
| A.有溶质析出 | B.溶液中Ca2+的数目不变 |
| C.溶剂的质量减小 | D.溶液的pH不变 |