火箭推进器常以联氨(N2H4) 为燃料、过氧化氢为助燃剂。已知下列各物质反应的热化学方程式:
N2H4(g)+O2(g)=N2(g)+2H2O(g) ΔH1=-533.23 kJ·mol-1
H2O(g)=H2O (l) DH2=–44 kJ·mol-1
2H2O2(l)=2H2O(l)+ O2(g) DH3=–196.4 kJ·mol-1
则联氨与过氧化氢反应的热化学方程式可表示为
| A.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l)ΔH=+817.63 kJ·mol-1 |
| B.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g)ΔH=-641.63 kJ·mol-1 |
| C.N2H4(g)+2H2O2(l)= N2(g)+4H2O(l)ΔH=-641.63 kJ·mol-1 |
| D.N2H4(g)+2H2O2(l)= N2(g)+4H2O(g)ΔH=-817.63 kJ·mol-1 |
下列对化学反应的认识正确的是
| A.化学反应必然引起物质状态的变化 |
| B.化学反应一定有化学键的断裂和生成 |
| C.需要加热的反应一定是吸热反应 |
| D.若反应物的总能量高于生成物的总能量,则该反应是吸热反应 |
下列各组化合物均属于烃的衍生物且只用水就可以区分的是
A. -CH3与 -CH3与 -NO2 -NO2 |
B. -NO2与 -NO2与 -Br -Br |
| C.CH2BrCH2Br与CH3CH2OH |
D.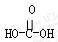 与CH3CH2Br 与CH3CH2Br |
分子式为C10H14的单取代苯的同系物,其可能结构有
| A.5种 | B.4种 | C.3种 | D.2种 |
下列有机物的命名正确的是
A.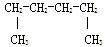 1,4 一二甲基丁烷 1,4 一二甲基丁烷 |
B.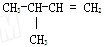 3-甲基丁烯 3-甲基丁烯 |
| C.CH2Cl-CH2Cl二氯乙烷 |
D.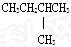 2-甲基丁烷 2-甲基丁烷 |
某种气态烃气体0.1 mol,完全燃烧得0.2mol CO2和3.6 g H2O,下列关于该气体的说法正确的是( )
| A.乙烯 | B.丙烯 |
| C.甲烷 | D.乙烷 |