下列物质按只含离子键、只含共价键、既含离子键又含共价键的顺序排列的是
| A.氯气 二氧化碳 氢氧化钠 | B.氯化钠 氦气 氢氧化钠 |
| C.氯化钠 过氧化钠 氯化铵 | D.氯化钠 过氧化氢 氯化铵 |
分类是化学学习与研究的常用方法,下列分类正确的是
| A.Na2O2、MgO、Al2O3均属于碱性氧化物 |
| B.纯碱、烧碱、熟石灰均属于碱 |
| C.酸、碱、盐之间发生的反应均属于复分解反应 |
| D.混合物、分散系、胶体从属关系如图所示 |

为确定某溶液的离子组成,进行如下实验:
①测定溶液的pH,溶液显强碱性
②取少量溶液中入稀盐酸至溶液呈酸性,产生无刺激性、能使澄清石灰水变浑浊的气体
③在上述溶液中再滴加Ba(NO3) 3溶液,产生白色沉淀
④取上层清液继续滴加Ba(NO3) 3溶液至无沉淀时,再滴加AgNO3溶液,产生白色沉淀
根据实验以下推测正确的是 ()
| A.一定有SO32-离子 | B.一定有CO32-离子 |
| C.Cl-离子一定存在 | D.不能确定HCO3-离子是否存在 |
高铁酸钠(Na2FeO4)是一种新型、高效、多功能水处理剂,是比Cl2、O3、ClO2、KMnO4氧化性更强、无二次污染的绿色水处理剂。工业制高铁酸钠的方法有如下两种:
湿法制备的主要离子反应为:2Fe(OH)3 +3ClO—+4OH—=2FeO42—+3Cl—+5H2O ,
干法制备的主要反应方程为:2FeSO4 +6Na2O2 = 2Na2FeO4 +2Na2O +2Na2SO4 +O2↑
则下列有关说法不正确的是()
| A.高铁酸钠中铁显+6价 |
| B.湿法中FeO42—是氧化产物 |
| C.干法中每生成1mol Na2FeO4转移4mol电子 |
| D.K2FeO4可氧化水中的H2S、NH3,生成的Fe(OH)3胶体还能吸附悬浮杂质 |
下列离子在溶液中能大量共存,加入(NH4)2Fe(SO4)2•6H2O晶体后,仍能大量共存的是
| A.Na+、H+、Cl-、NO3- | B.Na+、Mg2+、Cl-、SO42- |
| C.K+、Ba2+、OH-、I- | D.Cu2+、CO32-、Br-、ClO- |
下列离子方程式与所述事实相符且正确的是 ( )
| A.漂白粉溶液在空气中失效:ClO-+CO2+H2O =HClO+HCO3- |
B.用浓盐酸与MnO2反应制取少量氯气: MnO2+2H++2Cl- 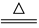 Mn2++Cl2↑+2H2O Mn2++Cl2↑+2H2O |
| C.用小苏打治疗胃酸过多:HCO3-+H+=CO2↑+H2O |
| D.在强碱溶液中次氯酸钠与Fe(OH)3反应生成Na2FeO4: |
3ClO-+2Fe(OH)3 =2FeO42-+3Cl-+H2O+4H+