小明见妈妈买了些取暖袋,他很好奇,打开了一袋,发现里面是黑色的粉末。那么,取暖袋里是什么物质在发生反应、释放热量呢?
【查找资料】
①取暖袋由原料层、明胶层、无纺布袋三部分组成。原料层中的黑色粉末的主要成分是铁粉、活性炭、蛭石、可溶性无机盐、吸水性树脂(含水)。
②蛭石是当今世界首屈一指的保温材料,起保温作用;吸水性树脂可反复释水、吸水,起吸水、保水的作用;二者均不参加反应。
③使用时应注意:不使用产品时请勿拆开密封包装。
【提出猜想】
①可溶性无机盐可能是氯化钠、硫酸钠、碳酸钠中一种或几种。
②取暖袋发热时,可能是铁粉、氧气、无机盐、水、活性炭几种物质间发生了化学反应。
【实验准备】
用NaCl溶液、Na2SO4溶液、Na2CO3溶液进行如下实验,为确定无机盐的成分提供参考。
| |
NaCl溶液 |
Na2SO4溶液 |
Na2CO3溶液 |
| 加入稀盐酸 |
无明显变化 |
无明显变化 |
现象Ⅰ |
| 加入BaCl2溶液 |
无明显变化 |
产生白色沉淀 |
产生白色沉淀 |
| 加入AgNO3溶液 |
产生白色沉淀 |
溶液略呈浑浊 |
产生淡黄色沉淀 |
(1)现象I是 。
(2)BaCl2溶液与Na2SO4溶液混合发生复分解反应,则白色沉淀的化学式为 。
【实验过程】
分别取没有使用的取暖袋和失效后的取暖袋中的黑色粉末完成以下实验,探究无机盐
的成分及参加反应的物质。
| 序号 |
加入试剂及操作 |
没有使用的暖袋 |
失效后的暖袋 |
| I |
加入足量水观察 |
无色溶液,大量固体在烧杯底部 |
无色溶液,大量固体在烧杯底部 |
| Ⅱ |
取I中上层清液,向其中滴加盐酸 |
无变化 |
无变化 |
| Ⅲ |
取I中上层清液,向其中滴加BaCl2溶液 |
无变化 |
无变化 |
| Ⅳ |
取I中上层清液,向其中滴加AgNO3溶液 |
白色沉淀 |
白色沉淀 |
| Ⅴ |
另取黑色粉末加入足量盐酸 |
大量气泡,溶液呈浅绿色 |
无气泡,溶液呈黄色溶液 |
(3)实验V中,观察到产生大量气泡和浅绿色溶液的反应的化学方程式是 。
(4)通过上述实验,可以得出以下结论:
①取暖袋中无机盐的成分是 。
②取暖袋发热时,原料层中一定参加反应的物质是 。
(5)利用右图装置,设计实验方案探究氧气是否参加了反应: ,则氧气参加了反应。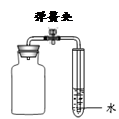
【反思与评价】
(6)小明根据IV中的现象判定无机盐未参加反应。他的结论是否合理,说明理由: 。
小雨同学阅读课外资料得知,双氧水分解除了二氧化锰作催化剂,还可以用氧化铜等物 质作催化剂,于是她对氧化铜产生了探究兴趣。
【提出问题】氧化铜是否也能作氯酸钾分解的催化剂?它是否比二氧化锰催化效果更好?
【设计实验】小雨以生成等体积的氧气为标准,设计了下列三组实验:(其他可能影响 实验的因素均忽略)
| 实验序号 |
KClO3质量 |
其他物质质量 |
待测数据 |
| ① |
1.2g |
||
| ② |
1.2g |
CuO 0.5g |
|
| ③ |
1.2g |
MnO2 0.5g |
(1)上述实验测量的“待测数据”是。
(2)若实验②比实验①的“待测数据”更(填“大”或“小”),说明氧化铜能加快氯酸钾的分解速率。
(3)对实验②反应后的固体加水溶解、过滤、洗涤、干燥,称量得到0.5g黑色粉末,经进一步实验证实过滤所得的黑色固体粉末为氧化铜。
【预期结论】氧化铜还能作氯酸钾分解的催化剂。
【评价设计】你认为小雨设计实验③和实验②对比的目的是。
【实验拓展】小雨同学从课外资料上还获得下列信息:氧化铁、硫酸铜、猪肝、马铃薯等也可以作过氧化氢分解的催化剂。下列有关催化剂的说法正确的是。
A.二氧化锰一定是催化剂
B.同一个反应可能有多种催化剂
C.催化剂一定是加快反应速率
D.也存在减慢反应速率的催化剂
E.对一定量的反应物来说,催化剂能改变生成物的质量
“滴水生火”魔术:向包有淡黄色过氧化钠(Na2O2)粉末的脱脂棉上滴加水,脱脂棉随即燃烧。某同学对该“魔术”很感兴趣,设计实验进行探究。
【提出问题】过氧化钠与水反应生成什么物质? 脱脂棉为什么会燃烧?
【实验1】取一支干燥的大试管,加入少量过氧化钠粉末,滴加蒸馏水,观察到试管内发生剧烈反应,产生大量气泡,用手触摸,试管底部发烫。
【提出猜想】生成的气体产物可能是:①;②。
【实验2】为探究气体产物,进一步设计并完成如下实验。
请完成表中空格:
| 操作 |
现象 |
结论 |
| 将带火星的木条伸入试管 |
带火星的木条复燃 |
气体产物是 |
【查阅资料】脱脂棉是经过化学处理去掉脂肪的棉花,极易燃烧;过氧化钠与二氧化碳反应生成碳酸钠和氧气。
【实验结论】
①过氧化钠与水的反应是反应(填“吸热”或“放热”)。
②脱脂棉燃烧的原因。
③扑灭由过氧化钠引发的火灾时,可以选择的灭火材料是。
A.二氧化碳 B.水 C.沙子
(本题共9分)碱式碳酸铜又称铜绿,是铜与空气中的氧气、二氧化碳和水等物质反应产生的物质。某化学兴趣小组同学发现Cu2(OH)2CO3受热分解后除生成CO2和 H2O外,试管中还有一些黑色粉末状固体。请结合所学知识,回答下列问题:
(1)若要证明有CO2和H2O生成,应选择下图的装置是(填字母序号);理由是。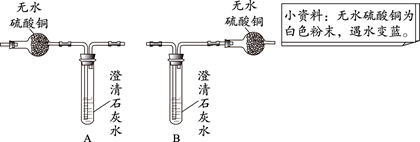
(2)探究黑色粉末的成分。
【猜想与假设】
该黑色粉末可能是①碳粉、②氧化铜、③;
小明同学经过认真分析,认为上述猜想一定不正确(填序号);其理由是;
【查阅资料】
a.碳粉与氧化铜均为不溶于水的黑色粉末;
b.氧化铜能与稀盐酸反应形成蓝色溶液;
c.碳粉既不与稀盐酸反应也不溶解在稀盐酸中。
【实验验证】
请你帮小组同学完成下述实验报告。
| 实验步骤 |
实验现象 |
实验结论 |
| 猜想②正确 |
(3)铜绿[Cu2 (OH)2CO3]受热分解的化学反应方程式:。
碳及许多含碳化合物不充分燃烧都要产生一氧化碳,一氧化碳是一种污染空气的有毒气体,它会使人中毒,通常采用燃烧法处理尾气中的一氧化碳。某同学对一氧化碳与一定量的氧气反应后所得的气体成分进行了如下实验探究:
【提出猜想】反应后气体的组成可能是:①CO和CO2;②只有CO2;③。
【实验探究】该同学为了验证自己的猜想,用下列装置进行实验: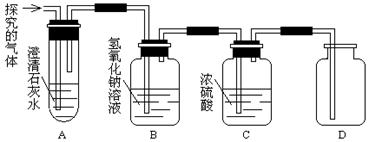
①装置B中氢氧化钠溶液的作用是;
②装置A中出现的现象是;
发生反应的化学方程式是;用带火星的木条伸入D中出现的现象是。
【实验结论】通过实验验证,猜想③成立。
如图所示,某兴趣小组在进行酸碱中和反应的实验探究时,向烧杯中氢氧化钠溶液中滴加稀盐酸一会儿后,发现忘记滴加指示剂。甲同学从烧杯中取少量反应后的溶液于一支试管中,并向试管中滴加几滴无色酚酞试液,振荡,观察到酚酞试液不变色。
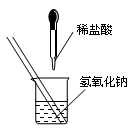
(1)请写出该中和反应方程式:。
猜想与假设:
【猜想一】甲同学:“两种物质已恰好完全中和,溶液呈中性”;
【猜想二】乙同学:“反应后氢氧化钠过量,溶液呈碱性”;
【猜想三】丙同学:。
甲、丙两位同学经过讨论后觉得乙同学的猜想不正确,两位同学的理由是:。
(2)设计并进行实验:
①为了验证自己的猜想,甲同学设计了以下实验方案:
| 实验步骤 |
实验现象 |
实验结论 |
| 用洁净干燥的玻璃棒蘸取少量反应后的溶液滴在干燥的pH试纸上,观察颜色变化并与标准比色卡对比。 |
pH_______(填“>”、“=”或“<”)7 |
猜想一不成立 |
②请你设计另一个实验(与甲同学方案不同)方案,验证丙同学的猜想,并填写下表:
| 实验步骤 |
实验现象 |
实验结论 |
| 猜想三: ______________ (填“成立”或“不成立”) |