某温度下,某实验小组在用粗锌(杂质难溶于水且与稀硫酸不反应)与200 g稀硫酸反应时,实验数据如下表所示。
| 实验 序号 |
粗锌的质量/g |
稀硫酸的质量/g |
生成气体的质量/g |
反应后溶液过滤,所得 固体烘干后的质量/g |
| 实验1 |
15 |
200 |
0.4 |
2 |
| 实验2 |
30 |
200 |
0.8 |
4 |
| 实验3 |
45 |
200 |
1.0 |
17.5 |
(1)上述实验中,粗锌中的锌有剩余的是 (填实验序号)。
(2)计算:实验3反应后溶液中硫酸锌的质量。
某校化学兴趣小组同学发现,长期使用的热水壶底部有一层水垢,水垢的主要成分是碳酸钙和氢氧化镁。他们为了测定水垢中碳酸钙的含量,将足量的盐酸加入到10g水垢中,产生CO2气体的情况如图所示。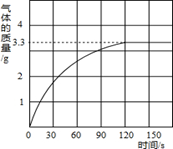
(1)从图中可以看出,10g水垢反应后生成的二氧化碳最多是g。
(2)水垢中的碳酸钙质量分数是多少?
为了测定未知浓度稀硫酸的溶质质量分数,取氢氧化钡溶液15g,逐滴加入该待测稀硫酸,同时测定并记录反应过程中混合溶液的pH变化情况(如图所示),过滤后得到滤液32.67g.
求:(1)反应后生成硫酸钡的质量是多少;
(2)该稀硫酸的溶质质量分数。
葡萄糖是生命活动中不可缺少的物质,它在人体内能直接参与新陈代谢过程。
| 部分性质 |
生理作用 |
|
| 葡萄糖 化学式: C6H12O6 |
白色结晶或颗粒状粉末,味甜;易溶于水;具有还原性,葡萄糖溶液与新制氢氧化铜悬浊液反应生成砖红色沉淀 |
葡萄糖为机体所需能量的主要来源,能促进肝脏的解毒功能,对肝脏有保护作用 |
请参与下列问题的讨论:
(1)葡萄糖中碳、氢、氧三种元素的质量比为。
(2)某兴趣小组的同学对葡萄糖的溶解性进行实验探究,其实验结果如图所示。实验说明了葡萄糖的溶解性除跟温度有关外,还与有关。现用10g纯净的葡萄糖,则理论上可配制5%的葡萄糖溶液g。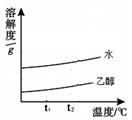
(3)该兴趣小组同学对某样品中葡萄糖的含量进行测定,反应原理为:C6H12O6+2Cu(OH)2 C6H12O7+Cu2O↓+2H2O
C6H12O7+Cu2O↓+2H2O
实验步骤如下:a.取样品20g于烧杯中,用蒸馏水溶解到50 mL;
b.加入新制的新制氢氧化铜悬浊液;
c.加热;
d.实验完毕后称得生成砖红色沉淀的质量为14.4g。计算该样品中葡萄糖的质量分数为多少? (请将计算过程写在答题纸上)
黄铜是铜和锌的合金,可以用来制造机器、电器零件及日用品。为了测定某黄铜样品中铜的质量分数,取20g该样品向其中加入一定量的稀硫酸,恰好完全反应,产生氢气的质量与加入稀硫酸的质量关系如图所示。
(1)完全反应后,生成H2的质量为g。
(2)完全反应后所得溶液的溶质质量分数是多少
(保留一位小数)?
下面是工厂苛化法生产烧碱的示意图。
(1)在实验室,操作Ⅰ的名称是;经操作Ⅰ得到废渣的主要成份是(写化学式)。
(2)物质X中各元素的质量比表示为。
(3)某工厂化验员向含有1.6 g氢氧化钠的溶液中,逐滴加入20.0 g盐酸至氢氧化钠和盐酸恰好完全反应。求盐酸中溶质的质量分数为多少?(写出过程)
(4)若用1.6 g上述得到的固体烧碱产品(含杂质)代替1.6 g氢氧化钠,逐滴加入上述相同浓度盐酸至反应物恰好完全反应,则消耗盐酸的质量20 g(填“大于”、“等于”或“小于”)。