下列各组离子,在溶液中能大量共存的是( )
| A.NO3-、Fe2+、Cl-、H+ | B.Na+、OH-、NH4+、AlO2- |
| C.Fe3+、NO3-、S2-、OH- | D.K+、OH-、Na+、S2- |
某有机物的分子模型如下图所示,则该有机物的名称可能为( )
| A.乙酸 | B.乙醇 | C.乙醛 | D.乙酸乙酯 |
关于苯的下列叙述中正确的是( )
| A.苯在催化剂的作用下能与液溴发生加成反应 |
| B.在苯中加入酸性MnO4溶液,振荡并静置后液体变为无色 |
| C.在苯中加入溴水,振荡并静置后下层液体为橙色 |
| D.在一定条件下苯能与氢气发生加成反应 |
下列各组中两个反应所属反应类型相同的是( )
| A.甲烷和氯气在光照下反应;乙烯能使溴水褪色 |
| B.乙烷在氧气中燃烧;由乙烯制取聚乙烯 |
| C.乙烯能使溴水褪色;乙烯能使酸性高锰酸钾溶液褪色 |
| D.乙烯和水反应制乙醇;乙烯能使溴水褪色 |
将甲烷与氯气混合,在光照下充分反应,所得产物有:①CH3Cl,②CH2Cl2,③CHCl3,④CCl4,⑤HCl。其中正确的是 ( )
| A.①⑤ | B.②⑤ |
| C.①②③的混合物 | D.①②③④⑤的混合物 |
下面是4个碳原子相互结合的6种方式(氢原子没有画出),其中符合通式CnH2n+2的是( )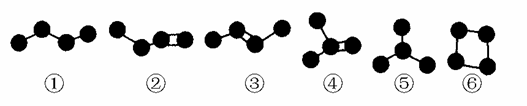
| A.②③ | B.①⑤ | C.②③④ | D.①⑤⑥ |