设NA为阿伏伽德罗常数的值,下列叙述正确的是( )
| A.28g乙烯和丙烯所含的碳原子数为为6NA |
| B.1L0.1mol•L-1乙酸溶液中H+数为0.1NA |
| C.1mol甲烷分子所含质子数为10NA |
| D.标准状况下,22.4L乙醇的分子数为NA |
现有部分短周期元素的性质或原子结构如下表:
| 元素编号 |
元素性质或原子结构 |
| T |
最外层电子数是次外层电子数的2倍 |
| X |
L层有三个未成对电子 |
| Y |
L层p电子数比s电子数多两个 |
| Z |
元素的最高正价为+7价 |
下列说法正确的是
A.Z离子的结构示意图为: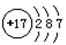 |
B.分子TY2的键角为180° |
C.T元素在周期表中的表示为: |
D.XZ3为非极性分子 |
下列说法正确的是
| A.乙硫醇(CH3CH2-SH)比乙醇(CH3CH2-OH)熔点低原因是乙醇分子间易形成氢键 |
| B.氯化钠易溶于水是因为形成了氢键 |
| C.氨易液化与氨分子间存在氢键无关 |
| D.H2O是一种非常稳定的化合物,这是由于氢键所致 |
下面排序不正确的是
| A.晶体熔点由低到高:CF4<CCl4<CBr4<CI4 | B.硬度由大到小:金刚石>碳化硅>晶体硅 |
| C.熔点由高到低:Na>Mg>Al | D.熔点由高到低: NaF> NaCl> NaBr>NaI |
下列有机物中含有两个手性碳原子的是
下列说法,正确的是
| A.离子键具有饱和性和方向性 |
| B.范德华力是分子间作用力的一种,氢键不属于分子间作用力 |
| C.s轨道与s轨道之间可以在任何方向上成键,所以共价键都没有方向性 |
| D.s轨道与p轨道只有沿着一定的方向,才能发生最大程度的重叠,形成共价键 |