如图所示是元素周期表的一部分,X、Y、Z、W均为短周期元素,若w原子最外层电子数是其内层电子数的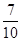 ,则下列说法中不正确的是( )
,则下列说法中不正确的是( )
| A.最高价氧化物对应水化物的酸性:W > Z |
| B.Y元素 的两种同素异形体在常温下都是气体 |
| C.原子半径由大到小排列顺序:Z >Y >X |
| D.气态氢化物的稳定 性:Y > X |
反应2A(g) 2B(g)+E(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
2B(g)+E(g)(正反应为吸热反应)达到平衡时,要使正反应速率降低,A的浓度增大,应采取的措施是
| A.降温 | B.减压 | C.减少E的浓度 | D.加压 |
下列有关硫酸工业制法的说法中错误的是
| A.预热从接触室出来的混合气体,有利于被浓硫酸吸收 |
| B.黄铁矿在加入沸腾炉前需粉碎,其目的是提高原料的利用率 |
| C.SO2跟O2是在催化剂(如V2O5等)表面上接触时发生反应的 |
| D.用98.3%的硫酸吸收SO3,而不用H2O或稀硫酸吸收SO3 |
对于可逆反应A(g)+B(g) 2C(g)+D(g)—Q当达到平衡后,在其
2C(g)+D(g)—Q当达到平衡后,在其
他条件不变时,若增大压强。以下说法正确的是
| A.正反应速度增大,逆反应速度增大,平衡向正反应方向移动 |
| B.正反应速度增大,逆反应速度减小,平衡向正反应方向移动 |
| C.正反应速度增小,逆反应速度增大,平衡向逆反应方向移动 |
| D.正反应速度减大,逆反应速度增大,平衡向逆反应方向移动 |
下列说法正确的是:
| A.可逆反应的特征是正反应速率总是和逆反应速率相等 |
| B.在其它条件不变时,升高温度可以使吸热反应速度增大,使放热反应速度减慢,所以升高温度可以使化学平衡向吸热反应的方向移动 |
| C.在其它条件不变时,增大压强一定会破坏反应的平衡状态 |
| D.在其它条件不变时,改变体系的温度能破坏大多数化学平衡状态 |
合成氨反应为:3H2+N2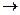 2NH3,当反应达到平衡时,其反应速率可以分别用V(H2),V(N2),V(NH3)表示,则正确的关系式是
2NH3,当反应达到平衡时,其反应速率可以分别用V(H2),V(N2),V(NH3)表示,则正确的关系式是
| A.v(H2)="v(N2)=v(NH3)" | B.v(H2)=3v(N2) |
| C.v(NH3)="3(H2)" | D.v(N2)=3V(H2) |