使1mol乙烯与氯气发生完全加成反应,然后使该加成反应的产物与足量氯气在光照的条件下发生取代反应,则两个过程中消耗的氯气的总的物质的量是 ( )
| A.3mol | B.4mol | C.5mol | D.6mol |
升高温度能加快反应速率的主要原因是
| A.活化分子能量明显增加 | B.降低活化分子的能量 |
| C.增加活化分子百分数 | D.降低反应所需要的能量 |
在一定条件下X2(g)+3Y2(g) 2Z3(g)达到化学平衡状态后,采取下列措施平衡不会发生移动的是
2Z3(g)达到化学平衡状态后,采取下列措施平衡不会发生移动的是
| A.充入X2 | B.缩小容器的体积 | C.升高温度 | D.使用催化剂 |
对于反应A(g)+3B(g) 2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
2C(g),下列各数据表示不同条件下的反应速率,其中反应进行得最快的是
A.v(A)=0.2mol/(L•s)B.v(B)=0.3mol/(L•s)
C.v(B)=0.2 mol/(L•s) D.v(C)=0.2mol/(L•s)
下列热化学方程式表达正确的是( 的绝对值均正确)
的绝对值均正确)
| A.C2H5OH(1)+3O2(g)=2CO2(g)+3H2O(g)△H="–1367.0" kJ/mol(燃烧热) |
| B.NaOH(aq)+HCl(aq)=NaCl(aq)+H2O(1)△H= +57.3kJ/mol(中和热) |
| C.S(s)+O2(g)=SO2(g)△H=–269.8kJ/mol(反应热) |
| D.2NO2=O2+2NO△H= +116.2kJ/mol(反应热) |
一定温度下在容积恒定的密闭容器中,进行如下可逆反应:A(s)+2B(g) 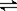 C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是
C(g)+D(g),当下列物理量不发生变化时,能表明该反应已达到平衡状态的是
①混合气体的密度②容器内气体的压强③混合气体的总物质的量
④B物质的量浓度⑤混合气体的平均相对分子质量⑥A的转化率
| A.①②③ | B.只有③ | C.②③④ | D.①④⑤⑥ |