已知硒与氧、硫同主族,与溴同周期,则下列关于硒的叙述中正确的是
| A.硒的原子序数为34 | B.硒的氢化物比HBr稳定 |
| C.硒的非金属性 比硫强 | D.硒的最高价氧化物的水化物显碱性 |
下列实验中,所选装置或实验设计合理的是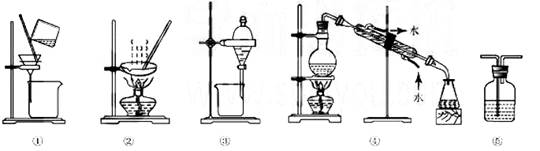
| A.图⑤ 所示装置中盛有饱和Na2SO3溶液除去SO2中含有的少量HCl |
| B.用乙醇提取溴水中的溴选择图③所示装置 |
| C.用图①和② 所示装置进行粗盐提纯 |
| D.用图④所示装置进行石油分馏实验制取丁烯 |
甲、乙两个电解池均以Pt为电极且互相串联。甲池盛有AgNO3溶液,乙池盛有一定量的某盐溶液,通电一段时间后,测得甲池阴极质量增加2.16g,乙池电极析出0.24g金属,则乙池中溶质可能是
| A.CuSO4 | B.MgSO4 | C.Al(NO3)3 | D.Na2SO4 |
在C6H10O2的所有同分异构体中,能与Na2CO3溶液反应产生CO2气体的且能使溴的四氯化碳溶液褪色的有(不考虑顺反等立体异构)
| A.8种 | B.13种 | C.17种 | D.21种 |
茶叶中铁元素的检验可经以下四个步骤完成,各步骤中选用的实验用品不能都用到的是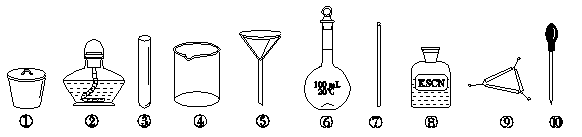
| A.将茶叶灼烧灰化,选用①、②和⑨ |
| B.用浓硝酸溶解茶叶并加蒸馏水稀释,选用④、⑥和⑦ |
| C.过滤得到滤液,选用④、⑤和⑦ |
| D.检验滤液中的Fe3+,选用③、⑧和⑩ |
化学中有许多物质之间的反应符合下列关系图,图中其他产物及反应所需条件均已略去。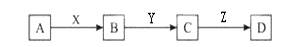
下列说法正确的是
| A.若X、Y为Fe,Z是氢氧化钠则D可能为氢氧化铁 |
| B.若X为NaOH,Y、Z为氧气,则D一定为酸性氧化物 |
| C.若X、Y为O2,Z为水则D一定为H2SO4 |
| D.若X、Y、Z全为O2符合条件的A不止一种 |