香叶醇是合成玫瑰香油的主要原料,其结构简式如下,下列有关香叶醇的叙述正确的是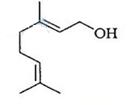
| A.香叶醇的分子式为C10H18O |
| B.不能使溴的四氯化碳溶液褪色 |
| C.不能使酸性高锰酸钾溶液褪色 |
| D.能发生加成反应不能发生取代反应 |
研究性学习小组进行了一系列化学实验后,发现高锰酸钾及其分解后的含锰元素的化合物都能和浓盐酸反应制得氯气,且含锰化合物的还原产物都是MnCl2。他们将6.32g KMnO4粉末加热一段时间,也不知道高锰酸钾是否完全分解,收集到0. 112L气体后便停止加热了,冷却后放入足量的浓盐酸再加热,又收集到气体体积是(上述气体体积都折合成标准状况)
| A.0. 448L | B.2.240L | C.2.016L | D.无法确定 |
一定温度下的难溶电解质AmBn在水溶液中达到溶解平衡时。已知下表数据
| 物质 |
Fe(OH)2 |
Cu(OH)2 |
Fe(OH)3 |
| Ksp/25℃ |
8.0×10-16 |
2.2×10-20 |
4.0×10-38 |
| 完全沉淀时的PH值范围 |
≥9.6 |
≥6.4 |
3~4 |
对含等物质的量的CuSO4、FeSO4、Fe2(SO4)3的混合溶液的说法,不科学的是
A.向该混合溶液中逐滴加入NaOH溶液,最先看到红褐色沉淀
B.该溶液中c(SO42-):{c(Cu2+)+c(Fe2+)+c(Fe3+)}>5:4
C.向该溶液中加入适量氯水,并调节pH值到3~4后过滤,得到纯净的CuSO4溶液
D.向该溶液中加少量铁粉即能观察到红色固体析出
以下实验方法能达到目的的是
| A.皮肤上沾上少量苯酚可用稀NaOH溶液洗去 |
| B.少量金属钠可保存在盛有乙醇的试剂瓶中 |
| C.将海带灰用水浸泡,过滤后向滤液中通入氯气,用酒精可萃取出单质碘 |
| D.仅通过物质间的相互反应即可鉴别出AlCl3、NaOH、HCl、NaCl四种溶液 |
下列现象或反应的原理解释正确的是
| 现象或反应 |
原理解释 |
|
| A. |
铝箔在酒精灯火焰上加热熔化但不滴落 |
铝箔对熔化的铝有较强的吸附作用 |
| B. |
合成氨反应需在高温条件下进行 |
该反应为吸热反应 |
| C. |
镀层破损后,镀锡铁比镀锌铁易腐蚀 |
锡比锌活泼 |
| D. |
2CO=C+O2在任何条件下均不能自发进行 |
该反应△H>0,△S<0 |
下列操作不会发生先沉淀后溶解现象的是
| A.向AgNO3溶液中滴加氨水直至过量 | B.向硫酸铝溶液中滴加氨水直至过量 |
| C.向NaAlO2溶液中滴加稀盐酸直至过量 | D.向澄清石灰水中通入CO2直至过量 |