对于平衡体系,mA(气)+ nB(气)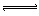 pC(气)+qD(气)+ Q有下列判断,其中正确的是
pC(气)+qD(气)+ Q有下列判断,其中正确的是
A.若温度不变,将容器的体积增大1倍,此时A的浓度变为原来的0.48倍,则m+ n> p+ q
B.若平衡时,A、B的转化率相等,说明反应开始时,A、B的物质的量之比为m∶n
C.若平衡体系共有气体a mol,再向其中加入b mol B,当重新达到平衡时,气体的总物质的量等于(a+b),则m+n=p+q
D.温度不变时,若压强增大至原来的2倍,达到新平衡时,总体积一定比原体积的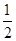 要小
要小
在实验室,称取一定量的粗盐经溶解、过滤、结晶等操作,可得到较纯净的食盐。下列图示对应的操作不规范的是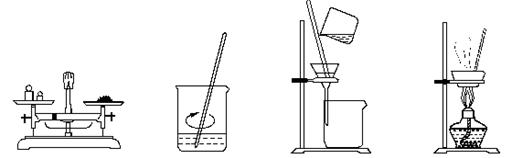
| A.称量 | B.溶解 | C.过滤 | D.结晶 |
下列有关物质性质的应用正确的是
| A.二氧化硫有漂白、杀菌性能,可在食品生产中大量使用 |
| B.二氧化硅具有较强的导电性,可用于制造光导纤维 |
| C.常温下铁能被浓硝酸钝化,可用铁质容器贮运浓硝酸 |
| D.金属钠具有强还原性,可用与TiCl4溶液反应制取金属Ti |
常温下,在下列给定条件的各溶液中,一定能大量共存的离子组是
| A.使酚酞变红色的溶液:NH4+、Ba2+、I-、Cl- |
| B.使甲基橙变红色的溶液:Fe3+、K+、NO3-、SO42- |
| C.含有0.1 mol·L-1 FeCl3溶液:Na+、K+、SCN-、NO |
| D.由水电离产生的c(H+)=10-12mol·L-1的溶液:Na+、K+、AlO2-、CO32- |
下列有关化学用语表示正确的是
A.苯甲醛: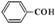 |
B.Mg2+的结构示意图: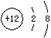 |
C.H2O2的电子式: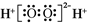 |
D.核内有8个中子的碳原子: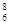 C C |
化学与生产、生活、环境等社会实际密切相关。下列叙述正确的是
| A.PM2.5表示每立方米空气中直径小于或等于2.5微米的颗粒物的含量,PM2.5值越低,大气污染越严重 |
| B.加强化石燃料的开采利用,能从根本上解决能源危机 |
| C.减少机动车尾气的排放,可以降低雾霾的发生 |
| D.加大以为动力的电动汽车的研发和推广,实现零污染。 |