25℃时,水的电离达到平衡:H2O H++OH-,下列叙述正确的是
H++OH-,下列叙述正确的是
| A.向水中加入氨水,平衡逆向移动,c(OH-)降低 |
| B.向水中加入少量固体硫酸氢钠,c(H+)增大,KW不变 |
| C.向水中加入少量固体CH3COONa,平衡逆向移动,c(H+)降低 |
| D.将水加热,KW增大,pH不变 |
在下列各微粒中,能使水的电离平衡向正方向移动,而且溶液的pH小于7是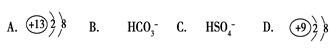
某浓度的氨水中存在下列平衡:NH3·H2O NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是
NH4++OH-,如想增大NH4+的浓度,而不增大OH-的浓度,应采取的措施是
| A.适当升高温度 | B.加入NH4Cl固体 |
| C.通入NH3 | D.加入少量NaOH |
下列离子反应方程式中,属于水解反应的是
A.CN-+H2O HCN+OH- HCN+OH- |
B.NH3·H2O NH4++OH- NH4++OH- |
C.HCO3-+H2O H3O++CO32- H3O++CO32- |
D.H2CO3 HCO3-+H+ HCO3-+H+ |
溶液中下列电离方程式书写正确的是
A.NaHSO4 Na++H++SO42- Na++H++SO42- |
B.NaHCO3===Na++H++CO32- |
| C.HClO===H++ClO- | D.H2S HS-+H+,HS- HS-+H+,HS- H++S2- H++S2- |
在室温下进行中和滴定,酸和碱恰好完全反应时,以下说法一定正确的是
| A.参加反应的酸和碱的物质的量相等 |
| B.参加反应的酸中的H+总量和碱中的OH-总量相等 |
| C.反应后混合液的pH=7 |
| D.不能用适当的酸碱指示剂来判断 |