下表是元素周期表一部分,列出了十个元素在周期表中的位置:
| 族 周期 |
IA |
IIA |
IIIA |
IVA |
VA |
VIA |
VIIA |
0 |
| 2 |
|
|
|
⑥ |
⑦ |
|
|
|
| 3 |
① |
③ |
⑤ |
|
|
|
⑧ |
⑩ |
| 4 |
② |
④ |
|
|
|
|
⑨ |
|
请用化学用语回答下列问题
(1)在③~⑦元素中,原子半径最大的是 (填元素符号);
(2)①~⑩中元素最高价氧化物对应的水化物中酸性最强的是 (填物质化学式),呈两性的氢氧化物是 (填物质化学式);
(3)⑦元素的最高价氧化物对应水化物与其氢化物能生成盐M,M中含有的化学键类型有 ;
(4)用电子式表示元素③与⑧形成化合物的过程 。
(5)写出含有32个电子的元素⑥的氢化物的分子式: 。
(6)写出工业冶炼⑤的化学方程式:
(7)写出将⑨元素单质从海水中(离子形式存在)提取所涉及到的三个步骤的离子方程式,第一步:Cl2+2Br-=2Cl-+Br2 第二步: ; 第三步Cl2+2Br-=2Cl-+Br2
化学学科中的平衡理论主要内容包括:化学平衡、电离平衡、水解平衡和溶解平衡等四种。且均符合勒夏特列原理。请回答下列问题。
(1)一定温度下,在一个固定容积的密闭容器中,可逆反应
A(g)+2B(g) 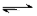 4C(g)
4C(g) H >0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
H >0达到平衡时,c(A)="2mol/L," c(B)="7mol/L," c(C)=4mol/L。试确定B的起始浓度c(B)的取值范围是;若改变条件重新达到平衡后体系中C的体积分数增大,下列措施可行的是
①增加C的物质的量②加压③升温④使用催化剂
(2)常温下,取pH=2的盐酸和醋酸溶液各100mL,向其中分别加入适量的Zn粒,反应过程中两溶液的pH变化如图所示。则图中表示醋酸溶液中pH变化曲线的是(填“A”或“B”)。设盐酸中加入的Zn质量为m1,醋酸溶液中加入的Zn质量为m2。则m1m2(选填“<”、“=”、“>”)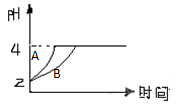
830K时,在密闭容器中发生下列可逆反应:
CO(g)+H2O(g) CO2(g)+H2(g)△H<0试回答下列问题:
CO2(g)+H2(g)△H<0试回答下列问题:
(1)若起始时c(CO)="2" mol·L-1,c(H2O)="3" mol·L-1,达到平衡时CO的转化率为60%,则在此温度下,该反应的平衡常数K=
(2)在相同温度下,起始物质按下列四种配比充入该容器中,c(H2O)=2mol·L-1,c(CO)=c(CO2)="1" mol·L-1, c(H2)="1.5" mol·L-1,则此时该反应是否达到平衡状态(选填“是”与“否”),此时v正v逆(选填“大于”、“小于”或“等于”)。
(3)平衡时若降低温度,该反应的K值将(选填“增大”、“减小”或“不变”),
平衡移动(选填“正向”、“逆向”或“不”)。
(1)在25℃、101kPa下,1g甲烷完全燃烧生成CO2和液态H2O,放出55 kJ的热量,写出表示甲烷燃烧热的热化学方程式:。
(2)2Zn(s)+O2(g)=2ZnO(s) ΔH1=" —702" kJ/mol
2Hg(l)+O2(g)=2HgO(s) ΔH2=" —182" kJ/mol
由此可知ZnO(s)+Hg(l)= Zn(s)+HgO(s)△H3=。
(3)20世纪30年代,Eyring和Pelzer在碰撞理论的基础上提出化学反应的过渡态理论:化学反应并不是通过简单的碰撞就能完成的,而是在反应物到生成物的过程中经过一个高能量过渡态。下图是NO2和CO反应生成CO2和NO过程中能量变化示意图,请写出NO2和CO反应的热化学方程式:。
根据下列信息写出符合要求的有机物的结构简式.
(1)某烃分子式为C6H14,若该烃不可能由炔烃与氢气加成得到,则该烃是__________________.
(2)有化学式均为C4H6的三种物质甲、乙、丙,甲中有三种氢原子,乙中只有一种氢原子,丙中有两种氢原子。乙分子的结构简式为;物质丙的结构简式为。
(3)某有机物A的蒸气对H2的相对密度为43,分子中C、H、O的原子个数之比为2∶3∶1。
A在酸性条件下水解可生成碳原子数相同的两种有机物。则A的结构简式为。在A的众多同分异构体中,属于不饱和羧酸的有3种,它们是CH2=CHCH2COOH、 、 。
(4) 某种一氯代物存在顺反异构,写出其中空间结构为“反式”的结构简式。
某种一氯代物存在顺反异构,写出其中空间结构为“反式”的结构简式。
葡萄糖是一种应用广泛的工业原料,由葡萄糖发酵得到的有机物A的分子结构模型如图所示
(1)当有机物分子中的碳原子通过四个单键与不同原子(或原子团)相连时,该碳原子为手性碳原子,则A中的手性碳原子有个。
(2)通过两种反应可以使A中的手性碳原子失去手性,写出反应的化学方程式。
①
②
(3)在一定条件下,两分子A能脱去两分子水形成一种六元环状化合物,写出该反应的方程式__________________________.
(4) A可以由丙烯经下列过程制得,E→B的反应类型为。C→D的反应类型为。
(5)酿酒工业上以葡萄糖为原料在酒化酶的作用下制得酒精。写出反应的化学方程式