生铁和钢的主要区别是( )
| A.生铁和钢的主要成分都是铁,但二者的含碳量不同,性能也不同。 |
| B.生铁和钢都是碳的合金 |
| C.生铁就是含杂质较多的钢,钢就是含杂质较少的生铁。 |
| D.生铁是混合物,钢是纯净物 |
下列关于苯酚的叙述中,正确的是
| A.苯酚呈弱酸性,能使紫色石蕊试液显浅红色 |
| B.苯酚能与FeCl3溶液反应生成紫色沉淀 |
| C.苯酚有强腐蚀性,沾在皮肤上可用水洗涤 |
| D.向少量苯酚溶液中滴加饱和溴水,可观察到白色沉淀 |
下列物质属于醇类的是
A. |
B. |
C.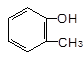 |
D. |
下列有机物的命名正确的是
| A.2,2—二甲基—1—丁烯 | B.3,3,4-三甲基戊烷 |
| C.2-甲基-3-乙基戊烷 | D.2-氯乙烷 |
下列有关化学用语不能表示2-丁烯的是( )
A.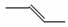 |
B.CH3CH=CHCH3 | C.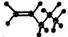 |
D.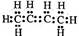 |
居室空气污染的主要来源之一是人们使用的装饰材料、胶合板、内墙涂料释放出的一种刺激性气味的气体,该气体是
| A.CH4 | B.NH3 | C.HCHO | D.SO2 |