如图利用培养皿探究氨气的性质。实验时向NaOH固体上滴几滴浓氨水,立即用另一培养皿扣在上面。下表中对实验现象所做的解释正确的是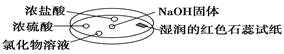
| 选项 |
实验现象 |
解释 |
| A |
浓盐酸附近产生白烟 |
NH3与HCl气体反应生成了NH4Cl固体 |
| B |
浓硫酸附近无明显现象 |
NH3与浓硫酸不发生反应 |
| C |
氯化物溶液变浑浊 |
该溶液一定是AlCl3溶液 |
| D |
湿润的红色石蕊试纸变蓝 |
NH3是一种可溶性碱 |
下列说法正确的是 ( )
| A.中和热一定是强酸跟强碱反应放出的热量 |
| B.1 mol酸与1 mol碱完全反应放出的热量是中和热 |
| C.在稀溶液中,酸与碱发生中和反应生成1 mol H2O时的反应热叫做中和热 |
| D.表示中和热的离子方程式为:H+(aq)+OH-(aq)=H2O(l); △H=57.3KJ/mol |
下列各组离子在给定条件的溶液中可能大量共存的是 ( )
| A.加入铝粉有大量氢气产生的溶液中:Mg2+、K+、NO3-、C1- |
| B.PH = 0的无色溶液中:Na+、K+、MnO4-、NO3- |
| C.在0.1mol/L的醋酸溶液中:Fe2+、Na+、ClO-、Ca2+ |
| D.在c(OH-)= 1×10-13的溶液中:NH4+、Ca2+、C1-、K+ |
化学与科学、技术、社会、环境密切相关。下列说法不正确的是( )
| A.家用铁锅用水清洗后放置在干燥处,能减弱电化学腐蚀 |
| B.加热能杀死甲型H1N1流感病毒是因为病毒的蛋白质受热变性 |
| C.某些抗酸药的主要成分是碳酸钠,作用是中和胃里过多的盐酸 |
| D.建国60周年燃放的焰火是某些金属元素焰色反应所呈现出来的色彩 |
在一定温度下的定容的容器中,当下列哪些物理量不再发生变化时,表明反应A(g)+2B(g)  C(g)+D(g)已达到平衡状态的是 ( )
C(g)+D(g)已达到平衡状态的是 ( )
①混合气体的压强②混合气体的密度③B的物质的量浓度④混合气体总物质的量⑤混合气体的平均相对分子质量⑥v(C)与v(D)的比值⑦混合气体总质量⑧混合气体总体积
A.①②③④⑤⑥⑦⑧ B. ①③④⑤ C.①②③④⑤⑦ D. ①③④⑤⑧
下列叙述正确的是()
| A.在原电池的负极和电解池的阴极上都是发生氧化反应 |
| B.铝比铁活泼,但铝制品比铁制品在空气中耐腐蚀 |
| C.用惰性电极电解饱和NaCl溶液,若有2mol电子转移,则生成1molNaOH |
| D.用惰性电极电解Na2SO4溶液,阴阳两极产物的物质的量之比为1:2 |