通常人们把拆开1mol某化学键吸收的能量看成该化学键的键能。键能的大小可以衡量化学键的强弱,也可以估计化学反应的反应热(ΔH),化学反应的ΔH等于反应中断裂旧化学键的键能之和与反应中形成新化学键的键能之和的差。下表是一些化学键的键能。
| 化学键 |
C—H |
C—F |
H—F |
F—F |
| 键能/(kJ·mol-1) |
414 |
489 |
565 |
155 |
根据键能数据估算下列反应CH4(g)+4F2(g)===CF4(g)+4HF(g)的反应热ΔH为
A.-1940kJ·mol-1 B.1940kJ·mol-1 C.-485kJ·mol-1 D.485kJ·mol-1
常温下,对于1L0.005mol·L-1硫酸表述中正确的是
| A.由水电离出的c(H+)=1.0×10-12mol·L-1 |
| B.加水稀释后,溶液中所有离子的浓度均减少 |
| C.2c(H+)= c(SO42-)+ c(OH-) |
| D.滴加稀氨水使pH=7,则c(NH4+)=" 2" c(SO42-) |
短周期元素中:A是地壳中含量最高的元素;B比Ne的质子数多1个;C最外层电子数与其电子层数相等;D单质是半导体材料;E非金属性在同周期元素中最强。下列说法中正确的是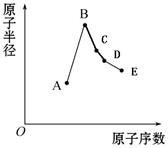
A.B离子的半径比C离子的半径小
B.A、B两单质反应可得到两种不同的离子化合物
C.C单质与A或E单质形成的化合物均为离子化合
D.B最高价氧化物对应的水合物与D单质发生反应能产生气体
从海带中提取碘的实验过程中,下列正确的操作是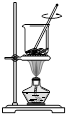


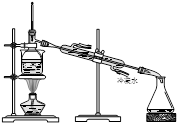
| A.海带灼烧成灰 | B.过滤含I-溶液 | C.放出碘的苯溶液 | D.分离碘并回收苯 |
下列说法不正确的是
| A.新制氯水可使蓝色石蕊试纸先变红后褪色 |
| B.浓硝酸在光照下发黄,说明浓硝酸不稳定 |
| C.SO2、NO2分别与水发生的反应均为氧化还原反应 |
| D.水泥、普通玻璃、陶瓷等都是传统的硅酸盐制品 |
设NA为阿伏加德罗常数的数值,下列说法正确的是
| A.1L0.1mol·L-1NaHSO3溶液中含有H+的数目为NA个 |
| B.常温常压下,等质量的CO2和N2O的气体体积相等 |
| C.60g组成为C2H4O2的有机物含C-H键数目为3NA个 |
| D.向稀HNO3溶液中加入过量的铁粉经充分反应后,转移的电子数目为3NA个 |