沐舒坦(结构简式为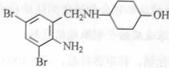 ,不考虑立体异构)是临床上使用广泛的。下图所示的是多条合成路线中的一条(反应试剂和反应条件均未标出)
,不考虑立体异构)是临床上使用广泛的。下图所示的是多条合成路线中的一条(反应试剂和反应条件均未标出)
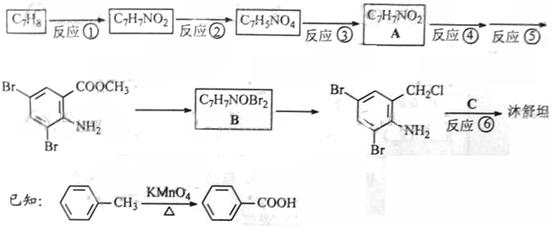
完成下列填空:
(1)写出反应试剂和反应条件。反应①
(2)写出反应类型。反应③
(3)写出结构简式。
(4)反应⑥中除加入反应试剂外,还需要加入,其目的是为了中和
防止
(5)写出两种的能发生水解反应,且只含3种不同化学环境氢原子的同分异构体的结构简式
(6) 反应②,反应③的顺序不能颠倒,其原因是
为确定某铝热剂(含氧化铁和铝)的组成,分别进行下列实验。
(1)若取ag样品,向其中加入足量的NaOH溶液,测得生成气体的体积(标准状况,下同)为b L 。反应的离子方程式为 。样品中铝的质量为 g。
(2)若使ag样品恰好完全反应,则反应中氧化铁与铝的质量比是 ,化学方程式为 。
(3)待(2)中生成物冷却后,加入足量盐酸,测得生成的气体体积为cL,该气体与(1)中所得气体的体积比c:b = 。
向浓度相等、体积均为50 mL的A、B两份NaOH溶液中,分别通入一定量的CO2后,再稀释到100 mL。在稀释后的溶液中逐滴加入0.1 mol/L的盐酸,产生CO2的体积 (标准状况)与所加盐酸的体积关系如右图所示。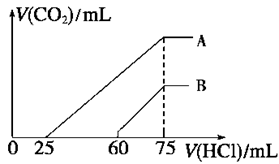
① A曲线表明,原溶液通入CO2后,所得溶质与盐酸反应产生CO2的最大体积是__________mL(标准状况);
②B曲线表明,原溶液通入CO2后,所得溶液中溶质的化学式为____________,物质的量之比为 ;
③原NaOH溶液的物质的量浓度为__________。
将过量的铜置入一定量的浓硝酸中,充分反应后放出11.2 L气体(标准状况下),试回答下列问题:
(1)反应放出的气体中,含有 (写化学式);
(2)写出反应过程中的的化学方程式: ;
(3)若有19.2g铜溶解,则参加反应的HNO3的物质的量 被还原HNO3的质量为
Ⅰ、碳元素是日常生活中接触非常多的一种元素,回答下列问题。
(1)用化学方程式表示溶洞生成的反应原理: 。
(2)可用稀盐酸来鉴别Na2CO3和NaHCO3溶液,现将稀盐酸慢慢滴入碳酸钠溶液中,请写出开始阶段发生反应的离子方程式 。
(3)写出用小苏打来治疗胃酸过多时发生反应的离子方程式: 。
II、氮元素在生命活动中扮演着重要的角色,回答下列与氮及其化合物有关的问题:
(1)德国化学家哈伯、波施等科学家成功地开发了将氮气转化为氨气的生产工艺。请用化学方程式表示工业合成氨的反应原理: 。
写出在氨气的出气口处,检验有氨气生成的操作:
(2)将氨气通入酚酞溶液中,酚酞溶液变成红色。请用方程式解释原因: 。
Ⅲ、印刷电路板是由塑料和铜箔复合而成,刻制印刷电路时要用FeCl3溶液作为“腐蚀液”溶解铜。
(1)写出该反应的离子方程式: ;
(2)从使用过的腐蚀液中可以回收金属铜,下列试剂能实现的是 (填序号)
| A.氯气 | B.铁 | C.硝酸 | D.稀硫酸 |
(3)向使用过的腐蚀液中通入Cl2,可使Fe2+转化为Fe3+,写出反应的离子方程式 。
A、B、C、D 4种元素,A元素所处的周期数、主族序数、原子序数均相等;B的原子半径是其所在主族中最小的,B的最高价氧化物对应水化物的化学式为HBO3;C元素原子的最外层电子数比次外层少2个;C的阴离子与D的阳离子具有相同的电子排布,两元素可形成化合物D2C。
(1)B元素的名称为___________;B在周期表中的位置是第___________周期第___________族。
(2)C的元素符号为______________,C的最高价氧化物的化学式为__________________。
(3)D的最高价氧化物对应的水化物的化学式为______________。