用含有、和少量的铝灰制备。,工艺流程如下(部分操作和条件略):
Ⅰ.向铝灰中加入过量稀,过滤:
Ⅱ.向滤液中加入过量溶液,调节溶液的约为3;
Ⅲ.加热,产生大量棕色沉淀,静置,上层溶液呈紫红色:
Ⅳ.加入至紫红色消失,过滤;
Ⅴ.浓缩、结晶、分离,得到产品。
(1)溶解的离子方程式是
(2) 氧化的离子方程式补充完整:

(3)已知:
生成氢氧化物沉淀的
| 开始沉淀时 |
3.4 |
6.3 |
1.5 |
| 完全沉淀时 |
4.7 |
8.3 |
2.8 |
注:金属离子的起始浓度为0.1
根据表中数据解释步骤Ⅱ的目的:
(4)己知:一定条件下, 可与反应生成,
① 向 Ⅲ 的沉淀中加入浓并加热,能说明沉淀中存在的现象是 .
②Ⅳ 中加入的目的是
常温下,将某一元碱BOH和HCl溶液等体积混合,两种溶液的浓度和混合后所得溶液的pH如下表:
| 实验编号 |
HCl的物质的量浓度 (mol·L-1) |
BOH的物质的量浓度 (mol·L-1) |
混合溶液的pH |
| ① |
0.1 |
0.1 |
pH=5 |
| ② |
c |
0.2 |
pH=7 |
| ③ |
0.1 |
0.2 |
pH>7 |
请回答:
(1)从第①组情况分析,BOH是(选填“强碱”或“弱碱”)。该组所得混合溶液中由水电离出的
c(OH—)=mol·L-1。
(2)第②组情况表明,c0.2。该混合液中离子浓度c(B+)c(Cl—)(选填“<”、“>”或“=”)。
(3)从第③组实验结果分析,混合溶液中(选填“<”、“>”或“=”)
甲:BOH的电离程度BCl的水解程度
乙:c(B+)—2 c (OH—)c(BOH)—2 c(H+)
图a是1 mol NO2和1 mol CO反应生成CO2和NO过程中能量变化示意图,图b是反应中的CO和NO的浓度随时间变化的示意图。根据图意回答下列问题:

a b
(1)写出NO2和CO反应的热化学方程式。
(2)从反应开始到平衡,用NO2浓度变化表示平均反应速率v(NO2)=。
(3)此温度下该反应的平衡常数K=;温度降低,K(填“变大”、“变小”或“不变”)
(4)若在温度和容积相同的三个密闭容器中,按不同方式投入反应物,测得反应达到平衡吋的有关数据如下表:
| 容器 |
甲 |
乙 |
丙 |
| 反应物投入量 |
1 mol NO2 1 mol CO |
2 mol NO 2 mol CO2 |
1 mol NO2、1 mol CO 1 mol NO、1 mol CO2 |
| 平衡时c(NO) /mol·L-1 |
1.5 |
3 |
m |
| 能量变化 |
放出a kJ |
吸收b kJ |
放出c kJ |
| CO或NO的转化率 |
α1 |
α2 |
α3 |
则:α1+α2=, a+b/2=,m=
化合物A是一种酯,它的分子式为C4H8O2,有下图转化关系。试回答下列问题。
(1)A的名称是。
(2)B的结构简式是。
(3)D中含有的官能团(填名称)。
(4)写出B和C生成A的化学方程式。
(1)固定和利用CO2能有效地利用资源,并减少空气中的温室气体。工业上有一种用CO2来生产甲醇燃料的方法:CO2(g)+3H2(g) CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。
CH3OH(g)+H2O(g)△H=-49.0kJ·mol-1。某科学实验将6molCO2和8molH2充入2L密闭容器中,测得H2的物质的量随时间变化如右图所示(实线)。图中数据a(1,6)代表的意思是:在l min时H2的物质的量是6mol。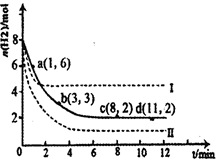
①下列时间段平均反应速率最大的是__________,最小的是______________。
| A.0~1min | B.1~3min | C.3~8min | D.8~11min |
②仅改变某一实验条件再进行两次实验测得H2的物质的量随时间变化如图中虚线所示,曲线Ⅰ对应的实验改变的条件是________,曲线Ⅱ对应的实验改变的条件是_________。
(2)利用光能和光催化剂,可将CO2和H2O(g)转化为CH4和O2。紫外光照射时,等量的CO2和H2O(g)在不同催化剂(Ⅰ、Ⅱ、Ⅲ)作用下,CH4产量随光照时间的变化如图所示。在0~30 h内,CH4的平均生成速率v(Ⅰ)、v(Ⅱ)和v(Ⅲ)从大到小的顺序为。反应开始后的12小时内,在第___________种催化剂的作用下,收集的CH4最多。
蛇纹石可用于生产氢氧化镁,简要工艺流程如下:
I.制取粗硫酸镁:用酸液浸泡蛇纹石矿粉,过滤;并在常温常压下结晶,制得粗硫酸镁(其中常含有少量Fe3+、Al3+、Fe2+等杂质离子)。
II.提纯粗硫酸镁:将粗硫酸镁在酸性条件下溶解,加入适量的0.1 mol·L-H2O2溶液,再调节溶液pH至7~8,并分离提纯。
III.制取氢氧化镁:向步骤II所得溶液中加入过量氨水。
已知:金属离子氢氧化物沉淀所需pH
| Fe3+ |
Al3+ |
Fe2+ |
Mg2+ |
|
| 开始沉淀时 |
1.5 |
3.3 |
6.5 |
9.4 |
| 沉淀完全时 |
3.7 |
5.2 |
9.7 |
12.4 |
请回答下列问题:
(1)步骤II中,可用于调节溶液pH至7~8的最佳试剂是(填字母序号)。
A. MgO B. Na2CO3 C. 蒸馏水
(2)Fe2+与H2O2溶液反应的离子方程式为。
(3)工业上常以Mg2+的转化率为考察指标,确定步骤III制备氢氧化镁工艺过程的适宜条件。其中,反应温度与Mg2+转化率的关系如右图所示。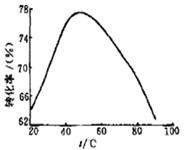
①步骤III中制备氢氧化镁反应的离子方程式为。
②根据图中所示50 ℃前温度与Mg2+转化率之间的关系,可判断此反应是
(填“吸热”或“放热”)反应。
③图中,温度升高至50 ℃以上Mg2+转化率下降的可能原因是。
④ Ksp表示沉淀溶解平衡的平衡常数。已知:
Mg(OH)2(s)  Mg2+ (aq)+ 2OH- (aq) Ksp = c(Mg2+)·c2(OH-) = 5.6×10-12
Mg2+ (aq)+ 2OH- (aq) Ksp = c(Mg2+)·c2(OH-) = 5.6×10-12
Ca(OH)2(s)  Ca2+ (aq) + 2OH- (aq)Ksp = c(Ca2+)·c2(OH-) = 4.7×10-6
Ca2+ (aq) + 2OH- (aq)Ksp = c(Ca2+)·c2(OH-) = 4.7×10-6
若用石灰乳替代氨水,(填“能”或“不能”)制得氢氧化镁,理由是。