用CuSO4•5H2O配制0.1 mol•L-1CuSO4水溶液,下面所列的方法正确的是 ( )
| A.取25 g CuSO4•5H2O溶于1 L水中 |
| B.将CuSO4•5H2O干燥去掉结晶水,取16 g溶于水制成1 L溶液 |
| C.将25 g CuSO4•5H2O溶于水制成1 L溶液 |
| D.取12.5 g CuSO4•5H2O溶于500 mL水中 |
下列关于化学反应的自发性叙述中正确的是 ( )
A.焓变小于0而熵变大于0的反应肯定是自发的
B.焓变和熵变都小于0的反应肯定是自发的
C.焓变和熵变都大于0的反应肯定是自发的
D熵变小于0而焓变大于0的反应肯定是自发的
下列叙述正确的是()
| A.将稀氨水逐滴加入稀硫酸中,当溶液pH=7时,c(SO42-)>c(NH4+) |
| B.两种醋酸溶液的物质的量浓度分别为c1和c2,pH分别为a和a+1,则c1=10c2 |
| C.pH=11的NaOH溶液与pH=3的醋酸溶液等体积混合,滴入石蕊溶液呈红色 |
D.向0.1 mol/L的氨水中加入少量硫酸铵固体,则溶液中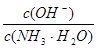 增大 增大 |
一定条件下,在体积为10 L的密闭容器中,1 mol X和1 mol Y进行反应:2X(g)+Y(g) Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
Z(g),经60 s达到平衡,生成0.3 mol Z,下列说法正确的是
| A.以X浓度变化表示的反应速率为0.001 mol/(L·s) |
| B.将容器体积变为20 L,Z的平衡浓度变为原来的1/2 |
| C.若增大压强,则物质Y的转化率减小 |
| D.若升高温度,X的体积分数增大,则该反应的DH>0 |
在0.1mol/L的CH3COOH溶液中存在如下电离平衡:
CH3COOH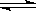 CH3COO-+H+对于该平衡,下列叙述正确的是
CH3COO-+H+对于该平衡,下列叙述正确的是
| A.加入少量NaOH固体,平衡向正反应方向移动 |
| B.加水,反应速率增大,平衡向逆反应方向移动 |
| C.滴加少量0.1mol/LHCl溶液,溶液中C(H+)减少 |
| D.加入少量CH3COONa固体,平衡向正反应方向移动 |
将pH为5的硫酸溶液稀释500倍,稀释后溶液中c (SO42-):c (H+)约为
| A.1:1 | B.1:2 | C.1:10 | D.10:1 |