下列热化学方程式正确的是(注:ΔH的绝对值均正确)( )
| A.C2H5OH(l)+3O2(g)===2CO2(g)+3H2O(g) ΔH=-1 367.0 kJ·mol-1(燃烧热) |
| B.Ba(OH)2(aq)+2HCl(aq)===BaCl2(aq)+2H2O(l) ΔH=-57.3 kJ·mol-1(中和热) |
| C.S(s)+O2(g)===SO2(g) ΔH=-269.8 kJ·mol-1(反应热) |
| D.2NO2===O2+2NO ΔH=+116.2 kJ·mol-1(反应热) |
下列各表中的数字代表的是原子序数,表中数字所表示的元素与它们在元素周期表中的位置相符的是
元素在同期表中的位置,反映了元素的原子结构和元素的性质。下列说法正确的是
| A.同一元素不可能既表现金属性,又表现非金属性 |
| B.第三周期元素的最高正化合价等于它所处的主族序数 |
| C.短周期元素形成离子后,最外层都达到8电子稳定结构 |
| D.同一主族的元素的原子,最外层电子数相同,化学性质完全相同 |
.已知A2-核内有x个中子,A原子的质量数为m,则n g A2-所含电子的总物质的量是
A.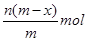 |
B.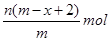 |
C. |
D.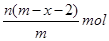 |
下列排列顺序正确的是
①沸点:H2Se>H2S>H2O②原子半径:Na>Mg>O
③酸性:H3PO4>H2SO4>HClO4④离子还原性:S2->Cl->Br-
| A.①③ | B.②④ | C.①④ | D.②③ |
下列各组性质比较的表示中,正确的是
| A.还原性:HF>HCI>HBr>HI | B.稳定性:HF<HCl<HBr<HI |
| C.与水反应由易到难:Cl2>Br2>I2>F2 | D.密度:F2<Cl2<Br2<I2 |