描述CH3—CH===CH—C≡C—CF3分子结构的下列叙述中,正确的是
①6个碳原子有可能都在一条直线上 ②6个碳原子不可能都在一条直线上
③6个碳原子都在同一平面上 ④6个碳原子不可能都在同一平面上
| A.①③ | B.②③ | C.①④ | D.②④ |
室温下向10mL pH=4的醋酸溶液中加入水稀释后,下列说法正确的是()
| A.溶液中粒子的数目减少 |
| B.再加入10mL pH=10的NaOH溶液,混合液pH=7 |
| C.醋酸的电离程度增大,c(H+)亦增大 |
D.溶液中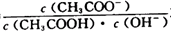 不变 不变 |
25℃时,在含有Pb2+、Sn2+的某溶液中,加入过量金属锡(Sn),发生反应: 体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
体系中c(Pb2+)和c(Sn2+)变化关系如图所示。下列判断正确的是
| A.往平衡体系中加入金属铅后,c(Pb2+)增大 |
| B.升高温度,平衡体系中c(Pb2+)增大 |
C.30℃时 ,该反应的平衡常数K>2.2 ,该反应的平衡常数K>2.2 |
| D.往平衡体系中加入少量Sn(NO3)2固体后,c(Pb2+)变小 |
控制适合的条件,将反应 设计成如图所示的原电池。下列判断不正确的是
设计成如图所示的原电池。下列判断不正确的是
| A.反应开始时,乙中石墨电极上发生氧化反应 |
| B.电流计读数为零后,在甲中溶入FeCl2固体, 乙中石墨电极为负极 |
| C.电流计读数为零时,反应达到化学平衡状态 |
| D.反应开始时,甲中石墨电极上Fe3+被还原 |
在温度t1和t2下,X2(g)和H2反应生成HX的平衡常数如下表:
下列说法正确的是
| A.在相同条件下随着卤素原子核电荷数的增加,平衡时X2的转化率逐渐降低 |
| B.t2>t1,HX的生成反应是吸热反应 |
| C.随着卤素原子核电荷数的增加HX的还原性逐渐减弱 |
| D.随着卤素原子核电荷数的增加HX的稳定性逐渐增强 |
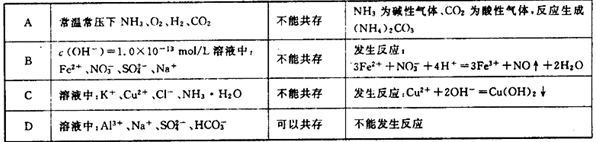
下列对各组离子或物质是否能够大量共存解释正确的是