下列化学反应方程式或离子方程式书写正确的是
| A.乙烯制溴乙烷: CH2CH2 + Br2→ CH2BrCH2Br |
B.乙醇催化氧化:2CH3CH2OH + O2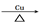 2CH3COH + 2H2O 2CH3COH + 2H2O |
C.苯与氢气加成: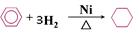 |
| D.从海带中提取碘:H2O2 + 2I- + 2H+ = I2 + 2H2O |
寿山石主要成分为叶蜡石,叶蜡石组成为Al2O3·4SiO2·H2O,下列观点不正确的是( )。
| A.寿山石雕刻作品要避免与酸、碱接触 |
| B.寿山石颜色丰富多彩是因为含有不同形态的金属氧化物 |
| C.潮湿的空气可能导致寿山石作品表面溶解变质 |
| D.置于干燥空气中可能会导致寿山石作品脱水变质 |
下列关于SiO2和CO2的叙述中不正确的是( )。
| A.都是共价化合物 |
| B.SiO2可用于制光导纤维,干冰可用于人工降雨 |
| C.都能溶于水且与水反应生成相应的酸 |
| D.都是酸性氧化物,都能与强碱溶液反应 |
下列说法正确的是( )。
| A.高温下,可在试管内完成焦炭和石英砂(SiO2)制取硅的反应 |
| B.CO2和钠在一定条件下反应可以得到金刚石和碳酸钠,反应中氧化剂和还原剂的物质的量之比是3∶4 |
| C.现代海战通过喷放液体SiCl4(极易水解)和液氨可产生烟幕,其主要成分是NH4Cl |
| D.从燃煤烟道灰中(含GeO2)提取半导体材料单质锗(Ge),没有发生氧化还原反应 |
在①浓硝酸;②水;③浓硫酸;④氢氟酸;⑤氢氧化钾溶液中,能与单质硅起化学反应的是( )。
| A.①② | B.②④ | C.④⑤ | D.③④ |
硅是构成无机非金属材料的一种主要元素,下列有关硅的化合物的叙述错误的是( )。
A.氮化硅陶瓷是一种新型无机非金属材料,其化学式为Si3N4
B.碳化硅(SiC)的硬度大,熔点高,可用于制作高温结构陶瓷和轴承
C.光导纤维是一种新型无机非金属材料,其主要成分为SiO2
D.二氧化硅为立体网状结构,其晶体中硅原子和硅氧单键的个数之比为1∶2