向甲、乙两恒温恒容的密闭容器中,分别充入一定量的A和B,发生反应:A(g)+B(g)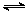 xC(g)+D(s)△H<0。测得两容器中c(A)随时间t的变化如图所示:
xC(g)+D(s)△H<0。测得两容器中c(A)随时间t的变化如图所示:
| 容器 |
甲 |
乙 |
| 容积(L) |
1 |
1 |
| 反应放热(kJ) |
a |
b |
| 反应物起始量 |
2 molA、2 molB |
1 molA、1 molB |
下列说法不正确的是
A.x=1
B.该温度下反应的平衡常数K=4
C.a=2b
D.保持其他条件不变,起始时向乙容器充入0.2 mol A、0.4 mol B、0.4 mol C、0.8molD,则此时v(正)> v(逆)
下列溶液中粒子的物质的量浓度关系正确的是
| A.0.1mol/L的KHA溶液,其pH=10,c(K+)>c(A2-)>c(HA-) >c(OH-) |
| B.0.1mol/L的氨水溶液与0.05mol/L H2SO4溶液等体积混合后所得溶液中: c(NH+4)+c(NH3)+c(NH3·H2O)=2c(SO42—) |
| C.0.1 mol/L的NaOH溶液与0.2 mol/L的HCN溶液等体积混合,所得溶液呈碱性: c (Na+)>c (HCN)>c (CN-)>c (OH-)>c (H+) |
| D.已知酸性HF > CH3COOH,物质的量浓度相等的NaF与CH3COOK溶液中: |
c(Na+) -c(F-) >c(K+) - c(CH3COO-)
设NA为阿伏伽德罗常数的值。下列说法正确的是
| A.5.6g铁粉在0.1mol氯气中充分燃烧,转移电子数为0.3NA |
| B.电解精炼铜时每转移NA个电子,阳极溶解32g铜 |
| C.标准状况下,18gH2O中含有的原子数目为3NA |
| D.室温下,31.0g白磷中含有的共价键数目为NA |
下列实验方案中,不能达到实验目的的是
| 选项 |
实验目的 |
实验方案 |
| A |
探究接触面积对化学反应速率的影响 |
相同温度下,取等质量的大理石块、大理石粉末分别投入等体积、等浓度的盐酸中 |
| B |
探究盐类的水解是吸热的 |
向醋酸钠溶液中滴入酚酞试液,加热后溶液红色加深 |
| C |
检验某溶液中是否含有Fe2+ |
向试样中滴加KSCN溶液,溶液颜色无变化,滴加氯水后溶液变红色 |
| D |
验证AgCl比AgI更难溶 |
向AgI沉淀中滴入稀KCl溶液,可观察有白色沉淀生成 |
能正确表示下列反应的离子方程式是
| A.向偏铝酸钠溶液中通入足量的CO2气体:AlO2-+CO2+2H2O=Al(OH)3↓+HCO3- |
| B.硫酸氢钠溶液中和氢氧化钡溶液至中性:SO42-+H++OH-+Ba2+=H2O+BaSO4↓ |
| C.少量铁溶于稀硝酸中:Fe+6H++3NO3-=Fe3++3NO2↑+3H2O |
| D.向污水中投放明矾,生成能凝聚悬浮物的胶体:Al3++3H2O=Al(OH)3(胶体)+3H+ |