元素化学性质随着原子序数的递增呈现周期性变化的原因是( )
| A.原子半径的周期性变化 | B.非金属性的周期性变化 |
| C.元素化合价的周期性变化 | D.原子核外电子排布的周期性变化 |
下列反应离子方程式正确的是()
| A.氨水中中通入过量二氧化硫: 2NH3·H2O + SO2= 2NH4+ + SO32-+ 2H2O |
| B.浓硫酸与Cu片反应中: Cu + SO42-+4H+= Cu2+ + SO2↑+2H2O |
| C.向澄清石灰水中加入少量小苏打溶液:Ca2+ + OH-+ HCO3-=CaCO3↓+ H2O |
| D.溴化亚铁溶液中通入过量氯气:Fe2+ + 2Br- + 2Cl2= Fe3+ + Br2 + 4Cl-氨水 |
下列关于原子结构、元素性质的说法正确的是( )。
| A.金属与非金属组成的化合物中只含离子键 |
| B.ⅠA族的元素与VIIA族元素形成的化合物不一定是离子化合物。 |
| C.不同原子组成的纯净物一定是化合物。 |
| D.ⅠA 族元素的阳离子氧化性越强,其最高价氧化物对应水化物的碱性越强 |
用NA表示阿伏加德罗常数的值,下列说法中正确的是( )
| A.1L 0.1mol/L的氨水溶液中含有0.1NA氨气分子 |
| B.28克C2H4与C4H8的混合气中含原子数为2 NA |
| C.标准状况下,11.2L的甲醛中含有氢原子个数为NA |
| D.1mol硫在空气中完全燃烧总共转移3 NA电子 |
下图表示在密闭容器中反应:CO2(g)+C(s) 2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;
2CO(g)△H>0达到平衡时,由于条件改变而引起反应速度和化学平衡的变化情况,ab过程中改变的条件可能是;bc过程中改变的条件可能是;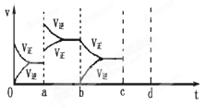
用铅蓄电池电解甲、乙电解池中的溶液。 电解一段时间后向c极和d极附近分别滴加酚酞试剂,c极附近溶液变红,下列说法正确的是()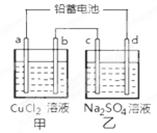
| A.d极为阴极 |
| B.若利用甲池精炼铜,b极应为粗铜 |
| C.放电时铅蓄电池负极的电极反应式为: PbO2(s) + 4 H+(aq)+SO4 2-(aq)+4e- = PbSO4 (s) +2H2O (l) |
| D.若四个电极材料均为石墨,当析出6.4 g Cu时,两池中共产生气体3.36 L(标准状况下) |