现有四种元素的基态原子,它们的核外电子排布式如下:
①1s22s22p63s23p4 ②1s22s22p63s23p3 ③1s22s22p3 ④1s22s22p5
则下列有关比较中正确的是
| A.第一电离能:④>③>②>① | B.原子半径:④>③>②>① |
| C.电负性:④>③>②>① | D.最高正化合价:④>③=②>① |
下列化学用语正确的是
①Na+的结构示意图 ②乙酸的分子式:CH3COOH
②乙酸的分子式:CH3COOH
③HC1O的电子式: ④葡萄糖的实验式:CH2O
④葡萄糖的实验式:CH2O
⑤聚乙烯的结构简式: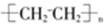 ⑥CO2的比例模型:
⑥CO2的比例模型:
| A.①②④ | B.②③⑥ | C.①④⑤ | D.③⑤⑥ |
以色列科学家发现准晶体独享2011年诺贝尔化学奖。已知的准晶体都是金属互化物。有关准晶体的组成与结构的规律仍在研究之中。人们发现组成为铝-铜-铁-铬的准晶体具有低摩擦系数、高硬度、低表面能以及低传热性,正被开发为炒菜锅的镀层;Al65Cu23Fe12十分耐磨,被开发为高温电弧喷嘴的镀层。下列说法正确的是
| A.离子化合物形成的晶体一定有金属元素 | B.合金是纯净物 |
| C.共价化合物中一定没有非极性键 | D.准晶体可开发成为新型材料 |
某含铬(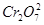 )废水用硫酸亚铁铵[
)废水用硫酸亚铁铵[ ]处理,反应中铁元素和铬元素
]处理,反应中铁元素和铬元素 完全转化为沉淀,该沉淀干燥后得到
完全转化为沉淀,该沉淀干燥后得到 ,不考虑处理过程中的实际损耗,下列叙述错误的是
,不考虑处理过程中的实际损耗,下列叙述错误的是
A.消耗硫酸亚铁铵的物质的量为 |
B.处理废水中的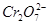 的物质的量为 的物质的量为 |
C.反应中发 生转移的电子数为 生转移的电子数为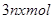 |
D.在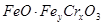 当中 当中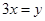 |
25℃时,下列关于分别由等体积 的2种溶液混合而成的溶液(忽略溶液体积
的2种溶液混合而成的溶液(忽略溶液体积 的变化)的说法中不正确的是
的变化)的说法中不正确的是
A. 溶液与 溶液与 溶液: 溶液: |
B.醋酸与 溶液: 溶液: |
C. 溶液与 溶液与 溶液: 溶液: |
D. 溶液与 溶液与 溶液: 溶液: |
阿魏酸在食品、医药等方面有广泛用途,一种合成阿魏酸的反应可表示为
下列说法正确的是
A.可用酸性 溶液检测上述反应是否有阿魏酸生成 溶液检测上述反应是否有阿魏酸生成 |
B.香兰素、阿魏酸均可与 、 、 、 、 溶液反应 溶液反应 |
| C.通常条件下,香兰素、阿魏酸都能发生取代、加成、消去反应 |
| D.与香兰素互为同分异构体,分子中有4种不同化学环境的氢,且能发生银镜反应的酚类化合物共有2种 |