下列是有关实验的叙述中,合理的是
①用托盘天平称取25.20 gNaCl固体
②用铁坩埚灼烧氢氧化钠固体
③使用容量瓶的第一步操作是先将容量瓶用蒸馏水洗涤后烘干
④用25 mL碱式滴定管量取14.80 mL 1 mol/L NaOH溶液
⑤用湿润的pH试纸测定某溶液的pH
⑥实验室配制氯化铁溶液时,可以先将氯化铁溶解在盐酸中,再配制到所需要的浓度
| A.②④⑥ | B.②③⑥ | C.①②④ | D.②③④⑤⑥ |
下列叙述正确的是
| A.容量瓶和量筒上均标有温度,且量筒和容量瓶均无“0”刻度 |
| B.用丁达尔现象可鉴别蛋白质溶液、葡萄糖溶液和淀粉溶液 |
| C.用洁净玻璃棒蘸取少量溶液,放在酒精灯上灼烧,透过蓝色钴玻璃观察K的焰色 |
| D.检验某溶液是否含有SO42-时,应取少量该溶液,依次加入BaCl2溶液和稀盐酸 |
与Ne的核外电子排布相同的离子跟与Ar核外电子排布相同的离子所形成的是化合物可以是
| A.MgBr2 | B.Na2S | C.CCl4 | D.KCl |
标准状况下,a L气体X2和b L气体Y2恰好完全反应生成c L气体Z,若2a=6b=3c,则Z的化学式为
| A.XY2 | B.X2Y | C.X3Y | D.XY3 |
下列除去杂质的方法正确的是
| A.除去N2中的少量O2:通过灼热的CuO粉末 |
| B.除去CO2中的少量HCl:通入Na2CO3溶液 |
| C.除去KCl溶液中的少量K2CO3:加入适量的盐酸 |
| D.除去KCl溶液中的少量MgCl2:加入适量NaOH溶液,过滤 |
下列实验装置图所示的实验操作,正确的是
A.干燥Cl2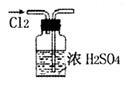 |
B.配制100ml0.1mol·L-1硫酸溶液 |
C.分离沸点相差较大的互溶液体混合物 |
D.分离互不相溶的两种液体 |