设NA为阿佛加德罗常数,下列叙述中正确的是( )
| A.46g NO2和N2O4混合气体中含有原子数为3NA |
| B.标准状况下22.4 L H2中含中子数为2NA |
| C.1L 1mol/L醋酸溶液中离子总数为2NA |
| D.1molFe与足量O2或Cl2反应均失去3NA个电子 |
向下列溶液中通入过量CO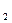 ,有固体析出的是()
,有固体析出的是()
①Ba(NO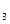 )
)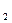 ②Na
②Na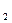 CO
CO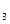 饱和溶液③氨化的饱和食盐水④CaCl
饱和溶液③氨化的饱和食盐水④CaCl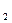
| A.①② | B.②③ | C.③④ | D.①④ |
钠和钾组成的合金4.6 g,与足量的水充分反应,得到H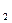 的质量可能是()
的质量可能是()
| A.0.29 g | B.0.18 g | C.2 g | D.1 g |
工业上常用氨碱法制取碳酸钠(将氨和二氧化碳先后通入饱和食盐水而析出小苏打,再经过滤、焙烧而得到纯碱),但却不能用氨碱法制碳酸钾,这是因为在溶液中()
A.KHCO 溶解度较大 溶解度较大 |
B.KHCO 溶解度较小 溶解度较小 |
C.K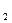 CO CO 溶解度较大 溶解度较大 |
D.K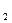 CO CO 溶解度较小 溶解度较小 |
关于铷的结构和性质的判断,正确的是()
①与水反应没有钠剧烈②它的原子半径比钠小③它的氧化物暴露在空气中易吸收二氧化碳④它是还原剂
| A.①② | B.③④ |
| C.②④ | D.① |
在空气中加热以下金属,生成M2O型氧化物的是()
| A.K | B.Cu | C.Li | D.Na |