碘溶于碘化钾溶液中形成I3—,并建立如下平衡:I3— I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
I—+ I2。实验室可以通过氧化还原滴定法测定平衡时I3—的浓度
实验原理:
为了测定平衡时的c(I3—) ,可用过量的碘与碘化钾溶液一起摇动,达平衡后取上层清液用标准的Na2S2O3滴定:2 Na2S2O3 + I2 =" 2NaI" + Na2S4O6。
由于溶液中存在I3— I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 = c(I2)+c(I3—);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3—)=c1 —c2;
I— + I2的平衡,所以用硫代硫酸钠溶液滴定,最终测得的是I2和I3—的总浓度,设为c1,c1 = c(I2)+c(I3—);c(I2) 的浓度可用相同温度下,测过量碘与水平衡时溶液中碘的浓度代替,设为c2,则c(I2)= c2,c(I3—)=c1 —c2;
实验内容:
1.用一只干燥的100 mL 碘量瓶和一只250 mL碘量瓶,分别标上1、2号,用量筒取80 mL 0.0100 mol.L-1 KI于1号瓶,取200 mL 蒸馏水于2号瓶,并分别加入0.5 g过量的碘。
2.将两只碘量瓶塞好塞子,振荡30分钟,静置。
3.分别取上层清液20 mL用浓度为c mol/L标准Na2S2O3溶液进行滴定。1号瓶消耗V1 mL Na2S2O3溶液,2号瓶消耗V2 mL Na2S2O3溶液。
4.带入数据计算c(I3—)
试回答下列问题
(1)标准Na2S2O3溶液应装入 (填“酸式滴定管”或“碱式滴定管”),原因是 。
(2)碘量瓶在震荡静置时要塞紧塞子,可能的原因是 。
(3)滴定时向待测液中加入的指示剂是 ,到达滴定终点时的现象为 。
(4)用c 、V1和V2表示c(I3—)为 mol·L-1。
(5)若在测定1号瓶时,取上层清液时不小心吸入了少量的I2固体,则测定的c(I3—) (填“偏大”、“偏小”或“不变”) 。
将一只铝制的易拉罐内充满二氧化碳,然后往罐内注入足量的NaOH溶液,立即用胶布密封罐口,经过一段时间后,罐壁凹瘪,又过一段时间后,瘪了的罐壁重新鼓起来。
(1)罐壁凹瘪的原因是;
反应的化学方程式是。
(2) 瘪罐重新鼓起来的原因是;
反应的离子方程式是。
有一种广泛用于汽车、家电产品上的高分子涂料,是按下列流程图生产的.流程图中:A和M(C3H4O)都可发生银镜反应,M和N的分子中碳原子数相同,A的烃基上的一氯代物有3种.
(1)写出下述物质的结构简式:A:________________,M:________________________.
(2)物质A的同类别的同分异构体为____________.
(3)N+B→D的化学方程式为________________________________________________.
(4)反应类型:X为__________,Y为__________.
感光性高分子也称为“光敏性高分子”,是一种在彩电荧光屏及大规模集成电路制造中应用较广的新型高分子材料,其结构简式为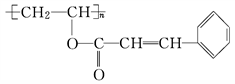
试回答下列问题:
(1)已知它是由两种单体经酯化后聚合而成的,试推断这两种单体的结构简式___________________________、______________________________;
(2)写出在(1)中由两种单体生成高聚物的化学反应方程式:___________________;
(3)对此高聚物的性质判断不正确的是________.
| A.在酸性条件下可以发生水解 |
| B.此高聚物不能使溴水褪色 |
| C.此高聚物可以使高锰酸钾酸性溶液褪色 |
| D.此高聚物可与溴水发生取代反应 |
E.此高聚物水解后可得到另一种高聚物
聚甲基丙烯酸羟乙酯的结构简式为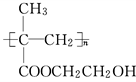 ,它是制作软质隐形眼镜的材料.
,它是制作软质隐形眼镜的材料.
(1)写出下列有关反应的化学方程式:
①由甲基丙烯酸羟乙酯制备聚甲基丙烯酸羟乙酯______________________________.
②由甲基丙烯酸制备甲基丙烯酸羟乙酯__________________________________.
③由乙烯制备乙二醇_____________________________________.
(2)请从它的结构上分析其作为隐形眼镜的材料的原因:___________________.
食品安全关系国计民生,影响食品安全的因素很多.下面是以食品为主题的相关问题,请根据要求回答.
聚偏二氯乙烯(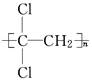 )具有超强阻隔性能,可作为保鲜食品的包装材料.它
)具有超强阻隔性能,可作为保鲜食品的包装材料.它
是由________(写结构简式)单体发生加聚反应生成的.若以乙炔为原料,通过加成反应生成1,1,2三氯乙烷,再和氢氧化钠醇溶液反应可合成这种单体,则在上述加成反应中宜选择的加成试剂是________.(选填编号字母)
| A.HCl | B.Cl2 |
| C.HClO | D.NaCl |