天津是我国研发和生产锂离子电池的重要基地。锂离子电池正极材料是含锂的二氧化钻(LiCoO2),充电时LiCoO2中Li被氧化,Li+迁移并以原子形式嵌入电池负极材料碳(C6)中,以LiC6表示。电池反应为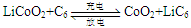 ,下列说法正确的是( )
,下列说法正确的是( )
| A.充电时,电池的负极反应为LiC6-e-=Li+C6 |
| B.放电时,电池的正极反应为CoO2+Li++e-=LiCoO2 |
| C.羧酸、醇等含活泼氢气的有机物可用作锂离子电池的电解质 |
| D.锂离子电池的比能量(单位质量释放的能量)低 |
下列物质中,只含有共价键的化合物是( )
| A.碘化氢 | B.烧碱 | C.液溴 | D.食盐 |
下列各组中互为同位素的是()。
A.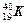 与 与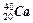 |
B.T2O与H2O | C.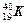 与 与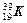 |
D.金刚石与石墨 |
下列各图中,表示正反应是吸热反应的图是()
某元素原子的最外层电子数为次外层电子数的3倍,则该元素原子核内质子数为 ( )
| A.3 | B.7 | C.8 | D.10 |
下列有关叙述正确的是( )
A.简单离子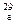 An+核外有x个电子,A的质量数可表示为2(x+n) An+核外有x个电子,A的质量数可表示为2(x+n) |
| B.Z为元素的某同位素En-,核外共有x个电子,又知此同位素原子质量数为A,则其原子核内的中子数为A-x-n |
| C.A元素的原子质量数为70,核内中子数为39,它的离子有28个电子,A元素氧化物的化学式为AO |
| D.跟9 g水中所含中子数相同的D2O的质量为8 g |