某有机物的结构简式如图所示,关于该物质的叙述错误的是( )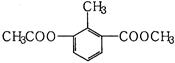
| A.一个分子中含有12个H原子 |
| B.苯环上的一氯代物有2种 |
| C.能使酸性KMnO4溶液褪色 |
| D.1mol该物质分别与足量H2、NaOH溶液反应,消耗其物质的量均为3mol |
设NA为阿佛加德罗常数,下列说法正确的是
①标准状况下,11.2L以任意比例混合的氮气和氧气所含的原子数为NA
②同温同压下,体积相同的氢气和氩气所含的分子数相等
③1L 2mol/L的氯化镁溶液中含氯离子为4NA
④标准状况下22.4LH2O中分子数为NA
⑤32g O2和O3混合气体中含有原子数为2NA
| A.①②③ | B.①②③⑤ | C.①③④ | D.③④ |
如果你家里的食用花生油混有水份,你将采用下列何种方法分离
| A.过滤 | B.蒸馏 | C.萃取 | D.分液 |
物质的量相同的甲烷(CH4)和氨气(NH3),可能相同的物理量是
| A.体积 | B.摩尔质量 | C.质量 | D.原子数 |
下列说法正确的是
| A.液态HCl不导电,所以HCl是非电解质 = |
| B.NH3、CO2的水溶液的导电,所以NH3 、CO2是电解质。 |
| C.铜、石墨均能导电,所以它们都是电解质。 |
| D.蔗糖在水溶液中或熔融时均不导电,所以是非电解质。 |
粗盐提纯实验用到的试剂中,不是为了除去原溶液中杂质离子的是
| A.碳酸钠溶液 | B.烧碱溶液 | C.盐酸 | D.氯化钡溶液 |