在一固定体积的密闭容器中加入2 mol A和1 mol B发生反应2A(g)+B(g) 3C(g)+D(g),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( )
3C(g)+D(g),达到平衡时C的浓度为w mol·L-1,若维持容器的体积和温度不变,按下列四种配比方案作为反应物,达平衡后,使C的浓度仍为w mol·L-1的配比是( )
| A.4 mol A+2 mol B | B.3 mol C+1 mol D+2mol A+1 mol B |
| C.3mol C+1 mol D+1 mol B | D.3 mol C+1 mol D |
下列叙述正确的是()
| A.已知Si—Si的键能为176KJ/mol,拆开1 mol晶体硅中的化学键所吸收的能量为176kJ |
| B.在CS2、PCl3分子中各原子最外层均达到8电子的稳定结构 |
| C.由同种元素组成的物质一定是纯净物 |
| D.干冰升华时,分子内共价键会发生断裂 |
前三周期元素中,基态原子中未成对电子与其所在周期数相同的元素有几种()
| A.3种 | B.4种 | C.5种 | D.6种 |
现代无机化学对硫-氮化合物的研究是最为活跃的领域之一。其中下图是已经合成的最著名的硫-氮化合物的分子结构。下列说法正确的是()
| A.该物质的分子式为SN |
| B.该物质的分子中既有极性键又有非极性键 |
| C.该物质具有很高的熔、沸点 |
| D.该物质与化合物S2N2互为同素异形体 |
有下列离子晶体空间结构示意图:●为阳离子,○为阴离子。以M代表阳离子,N代表阴离子,化学式为MN2的晶体结构为()

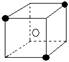

A B C D
下列说法中正确的是()
①所有基态原子的核外电子排布都遵循构造原理 ②同一周期从左到右,元素的第一电离能、电负性都是越来越大 ③金属键、共价键和氢键都具有相同的特征:方向性和饱和性 ④所有的配合物都存在配位键,所有含配位键的化合物都是配合物 ⑤所有含极性键的分子都是极性分子 ⑥所有金属晶体中都含有金属键 ⑦所有的金属晶体熔点肯定高于分子晶体
| A.③⑥⑦ | B.⑥ | C.③④⑤ | D.①②⑥⑦ |