反应2SO2+O2 2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
2SO3经一段时间后,SO3的浓度增加了0.4mol·L-1,在这段时间内用O2表示的反应速率为0.04mol·L-1·s-1,则这段时间为( )
| A.0.1s | B.2.5s | C.5s | D.10s |
化学美无处不在,下图是物质间发生化学反应的颜色变化,其中X是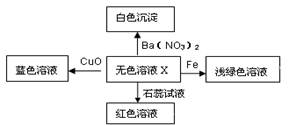
| A.稀盐酸 | B.稀硫酸 | C.硫酸钠溶液 | D.碳酸钠溶液 |
垃圾分类从你我他开始。废电池属于
A. B. C. D.
H2和I2在一定条件下能发生反应:H2(g) +I2(g) 2HI(g) △H=—a kJ·mol-1
2HI(g) △H=—a kJ·mol-1
已知: (a、b、c均大于零)
(a、b、c均大于零)
下列说法不正确的是
| A.反应物的总能量高于生成物的总能量 |
| B.断开1 mol H-H键和1 mol I-I键所需能量大于断开2 mol H-I键所需能量 |
| C.断开2 mol H-I键所需能量约为(c+b+a) kJ |
| D.向密闭容器中加入2 mol H2和2 mol I2,充分反应后放出的热量小于2a kJ |
下述实验方案能达到实验目的的是
| 编号 |
A |
B |
C |
D |
| 实验 方案 |
 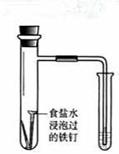 食盐水 |
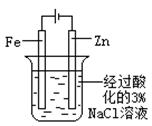 片刻后在Fe电极附近滴入K3[Fe(CN)6]溶液 |
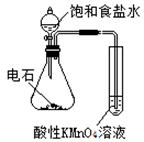 |
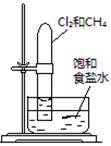 置于光亮处 |
| 实验 目的 |
验证铁钉发生 析氢腐蚀 |
验证Fe电极被保护 |
验证乙炔的还原性 |
验证甲烷与氯气发生 化学反应 |
有0.1 mol·L-1的三种溶液:①CH3COOH、②NaOH、③CH3COONa,下列说法正确的是
| A.溶液①中,c(CH3COO-)= c(H+) |
| B.溶液①、②等体积混合,混合液中c(CH3COO-)等于溶液③中的c(CH3COO- ) |
| C.溶液①、②等体积混合,混合液中c(CH3COO-)+c(CH3COOH)=c(Na+) |
| D.溶液①、③等体积混合,混合液中c(Na+)> c(CH3COO-)> c(H+)> c(OH-) |