NA表示阿伏加德罗常数的值,下列说法正确的是
| A.常温下,在18g18O2中含有NA个氧原子 |
| B.标准状况下,17g NH3所含共价键数为NA个 |
| C.标准状况下,22.4L苯的分子数约为NA个 |
| D.1mol Na2O2中含有的阴离子数目为2NA个 |
已知醋酸、醋酸根离子在溶液中存在下列平衡:
| CH3COOH+H2O |
C H3COO-+H3O+ |
K1=1.75×10-5 mol·L-1 |
| CH3COO-+H2O |
CH3COOH+OH- |
K2=5.71×10-10 mol·L-1 |


 现将 50 mL 0.2 mol·L-1醋酸与 50 mL 0.2 mol·L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是
现将 50 mL 0.2 mol·L-1醋酸与 50 mL 0.2 mol·L-1醋酸钠溶液混合制得溶液甲,下列叙述正确的是
A.溶液甲的pH>7
B.对溶液甲进行微热,K1、K2 同时增大
C.若在溶液甲中加入少量的 NaOH 溶液,溶液的 pH 明显增大
D.若在溶液甲中加入 5 mL 0.1 mol·L-1的盐酸,则溶液中醋酸的 K1 会变大
用 NA 表示阿伏伽德罗常数的值,下列叙述正确的是()
| A.22.4LCO2 与足量的 Na2O2 反应时,转移的电子数为 NA 个 |
| B.0.1mol 铁在 0.1molCl2 中充分燃烧,转移的电子数为 0.2NA 个 |
C.对于反应:A(g)+B(g)  C(g)+D(g)单位时间内生成 NA 个 A 分子时,同时消耗NA 个 C 分子,说明该反应一定达到最大限度 C(g)+D(g)单位时间内生成 NA 个 A 分子时,同时消耗NA 个 C 分子,说明该反应一定达到最大限度 |
| D.Zn -H2SO4-Cu 原电池中,当电路中有 NA 个电子通过时,溶液的质量增加 1g |
下列各对物质中,互为同系物的是()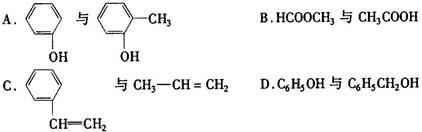
已知 298K 时,H+(aq)+ OH-(aq)= H2O(l) △H = -57.3 kJ/ mol ,推测含 1mol
CH3COOH 的稀溶液与含 1 mol NaOH 的稀溶液反应放出的热量()
| A.大于 57.3 kJ | B.等于 57.3 kJ | C.小于 57.3 kJ | D.无法确定 |
在 A+2B  3C+4D 反应中,表示该反应速率最快的是 ()
3C+4D 反应中,表示该反应速率最快的是 ()
A.v(A)=0.3 mol/(L·s) B.v(B)=0.5 mol/(L·s)
C.v(C)=0.8 mol/(L·s) D.v(D)=1 mol/(L·min)